题目内容
| 素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| V | 420 | 3100 | 4400 | 5900 |
| A、TCl |
| B、TCl2 |
| C、TCl3 |
| D、TCl4 |
考点:元素周期律和元素周期表的综合应用
专题:
分析:由元素的电离能可以看出,Q的电离能很大,可能为零族元素,R和U的第一电离能较小,第二电离能剧增,故表现+1价,最外层电子数为1,二者位于同一族,S的第一、第二电离能较小,第三电离能剧增,故表现+2价,最外层电子数为2,T的第一、第二、第三电离能较小,第四电离能剧增,表现+3价,最外层电子数为3.
解答:
解:由元素的电离能可以看出,Q的电离能很大,可能为零族元素,R和U的第一电离能较小,第二电离能剧增,故表现+1价,最外层电子数为1,二者位于同一族,S的第一、第二电离能较小,第三电离能剧增,故表现+2价,最外层电子数为2,T的第一、第二、第三电离能较小,第四电离能剧增,表现+3价,最外层电子数为3,T元素最高正价是+3价,形成的氯化物的化学式为TCl3.
故选C.
故选C.
点评:本题考查电离能知识,题目难度中等,注意原子的最外层电子数与电离能以及化合价的关系.

练习册系列答案
相关题目
已知:①2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O;②Cl2+2FeCl2═2FeCl3;③2KI+2FeCl3═2KCl+I2+2FeCl2.则下列判断正确的是( )
| A、氧化性:MnO4->Cl2>Fe3+>I2 |
| B、还原性:Fe2+>I->Cl- |
| C、FeCl3能使湿润的淀粉碘化钾试纸变蓝 |
| D、反应①中只体现盐酸的还原性 |
甲、乙、丙三种物质的溶解度曲线如图所示,下列说法错误的是( )


| A、50℃时,乙物质的溶解度是40g |
| B、30℃时,三种物质的溶解度:乙>甲>丙 |
| C、升温可使丙的不饱和溶液变饱和 |
| D、50℃时,将等质量的甲、丙两种物质的饱和溶液同时降温至10℃时,所得溶液的溶质质量分数:丙>甲 |
从经济效益和环境保护考虑,大量制取硝酸铜最适宜采用的方法是( )
| A、Cu+HNO3(浓)→Cu(NO3)2+NO2↑ |
| B、Cu+HNO3 (稀)→Cu(NO3)2+NO↑+H2O |
| C、Cu+O2→CuO,CuO+HNO3 (稀)→Cu(NO3)+H2O |
| D、Cu+AgNO3→Cu(NO3)2+Ag |
“人文奥运、科技奥运、绿色奥运”是2008年北京奥运会的重要特征.其中禁止运动员使用兴奋剂是重要举措之一.如图两种兴奋剂的结构分别为:则关于它们的说法中正确的是( )
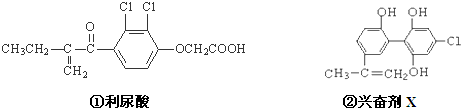
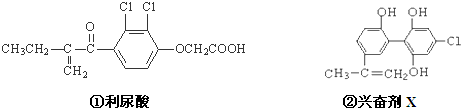
| A、利尿酸乙酯分子中有三种含氧官能团,在核磁共振氢谱上共有七个峰 |
| B、1 mol兴奋剂X与足量浓溴水反应,最多消耗4 mol Br2 |
| C、两种兴奋剂最多都能和含3molNaOH的溶液反应 |
| D、两种分子中的所有碳原子均不可能共平面 |
 如图是SO2与O2在接触室中多段催化氧化2SO2(g)+O2(g)?2SO3(g)+Q(Q>0)回答下列问题:
如图是SO2与O2在接触室中多段催化氧化2SO2(g)+O2(g)?2SO3(g)+Q(Q>0)回答下列问题: 某校化学兴趣小组的同学用滴定法对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,回答下列问题:
某校化学兴趣小组的同学用滴定法对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,回答下列问题: 影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究.
影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究.