题目内容
某化学反应2AB+D在四种不同条件下进行.B、D起始浓度为0.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:?| 实验序号 | 温度 | 0min | 10min | 20min | 30min | 40min | 50min | 60min |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 |
A.在实验1中,反应在10至20min时间内平均速率为0.013mol?-1
B.在实验2中,A的初始浓度c2=1.0mol/L,反应经20min就达到平衡,推测实验2中还可能隐含的条件是:使用了合适的催化剂
C.设实验3的反应速率为v3,实验1的反应速率为v1,则v3>v1,且c3>1.0mol/L
D.比较实验4和实验1,可推测该反应是放热反应
【答案】分析:A.根据V=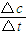 解题;
解题;
B.达到平衡的标志是浓度不再改变,催化剂呢过加快反应速率;
C.以10至20min为例求出反应速率进行比较;
D.加热平衡向吸热反应方向移动.
解答:解:A.在实验1中,反应在10至20min时间内平均速率为V=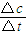 =
=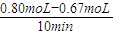 =0.013mol?(L?min)-1,故A正确;
=0.013mol?(L?min)-1,故A正确;
B.反应经20minA的浓度不再改变,说明达到平衡,较其他实验达到平衡时间最短,故使用了合适的催化剂,故B正确;
C.在实验1中,反应在10至20min时间内平均速率为V=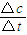 =
=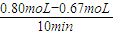 =0.013mol?(L?min)-1,在实验3中,
=0.013mol?(L?min)-1,在实验3中,
反应在10至20min时间内平均速率为V=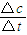 =
=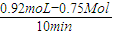 =0.015mol?(L?min)-1,,故v3>v1,在0min到10min内实验1中c=0.1mol/L,由平衡时浓度可知在实验3中c>0.1mol/L,故C正确;
=0.015mol?(L?min)-1,,故v3>v1,在0min到10min内实验1中c=0.1mol/L,由平衡时浓度可知在实验3中c>0.1mol/L,故C正确;
D.比较实验4和实验1可知平衡时实验4反应物A的浓度小,由实验1到实验4升高温度,平衡右移,加热平衡向吸热反应方向移动,故D错误.
故选D.
点评:本题考查反应速率的表示方法,化学平衡移动的判断,掌握反应速率的计算方法是解题的关键.
 解题;
解题;B.达到平衡的标志是浓度不再改变,催化剂呢过加快反应速率;
C.以10至20min为例求出反应速率进行比较;
D.加热平衡向吸热反应方向移动.
解答:解:A.在实验1中,反应在10至20min时间内平均速率为V=
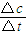 =
=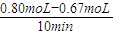 =0.013mol?(L?min)-1,故A正确;
=0.013mol?(L?min)-1,故A正确; B.反应经20minA的浓度不再改变,说明达到平衡,较其他实验达到平衡时间最短,故使用了合适的催化剂,故B正确;
C.在实验1中,反应在10至20min时间内平均速率为V=
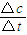 =
=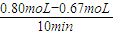 =0.013mol?(L?min)-1,在实验3中,
=0.013mol?(L?min)-1,在实验3中,反应在10至20min时间内平均速率为V=
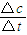 =
=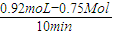 =0.015mol?(L?min)-1,,故v3>v1,在0min到10min内实验1中c=0.1mol/L,由平衡时浓度可知在实验3中c>0.1mol/L,故C正确;
=0.015mol?(L?min)-1,,故v3>v1,在0min到10min内实验1中c=0.1mol/L,由平衡时浓度可知在实验3中c>0.1mol/L,故C正确;D.比较实验4和实验1可知平衡时实验4反应物A的浓度小,由实验1到实验4升高温度,平衡右移,加热平衡向吸热反应方向移动,故D错误.
故选D.
点评:本题考查反应速率的表示方法,化学平衡移动的判断,掌握反应速率的计算方法是解题的关键.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
 B+D在四种不同条件下进行,B、D起始浓度为零.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为零.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:

 B + D在不同条件下进行,B、D的起始浓度为0,把反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示。
B + D在不同条件下进行,B、D的起始浓度为0,把反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示。
 www.k@s@5
www.k@s@5 @u.com
@u.com