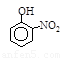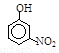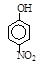题目内容
请回答下列问题:
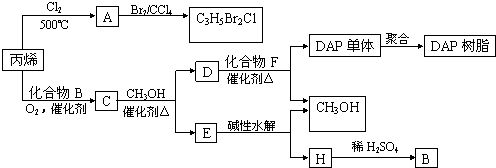
(1)组成丁的元素在周期表中的位置______.B的俗名______,C物质的用途之一______.
(2)写出A+乙
| △ |
(3)在加热条件下,丁与气态D可发生反应,该反应的化学方程式为______.
(4)若21.6g A与适量的乙反应生成B,A、B按上述图示转化为溶液I和溶液II(假设各步反应均恰好进行完全);向溶液I中通入______mol Cl2,经充分反应可恰好使溶质的组成与溶液II完全相同.
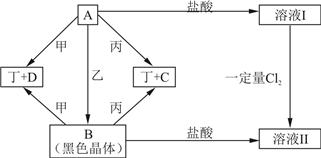
B为黑色晶体,B为Fe3O4,甲、乙为非金属单质,故甲、乙有一种为H2,一种为O2,原子序数总和为48,故另外元素的原子序数为48-1-8-26=13,为Al元素;
丙、丁为金属单质,由A+甲→丁+D及Fe3O4+甲→丁+D可知,丁为Fe,故丙为Al,A与Fe3O4含有相同的元素,甲为H2,D为H2O,故乙为O2,结合A
| 乙 |
FeO
| 盐酸 |
| 盐酸 |
(1)丁为Fe,Fe元素是26号元素,常用周期表中第四周期第Ⅷ族;
B为Fe3O4,俗名为磁性氧化铁;
C为Al2O3,可以作耐火材料或治炼铝的原料;
故答案为:第四周期第Ⅷ族;磁性氧化铁;作耐火材料或治炼铝的原料;
(2)A+乙
| △ |
| ||
故答案为:6FeO+O2
| ||
(3)在加热条件下,Fe与水蒸气反应生成四氧化三铁与氢气,反应方程式为:3Fe+4H2O(g)
| ||
故答案为:3Fe+4H2O(g)
| ||
(4)若21.6gFeO的物质的量为
| 21.6g |
| 72g/mol |
| 1 |
| 3 |
| 2 |
| 3 |
故答案为:0.1mol.

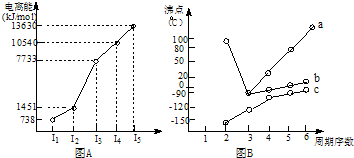
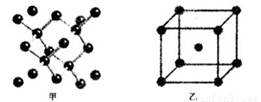
(18分)(1)I.短周期某主族元素M的电离能情况如右图(A)所示。则M元素位于周期表的第 族。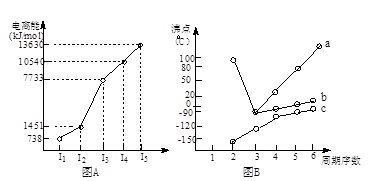
II.图B折线c可以表达出第 族元素氢化物的沸点的变化规律。两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线a和b,你认为正确的是:__________(填“a”或“b”)
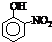
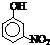
III.部分有机物的熔沸点见下表:
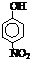
| 烃 | CH4 | CH3CH3 | CH3(CH2)2CH3 | 硝基苯酚 | 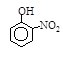 | 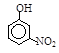 | 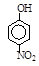 |
| 沸点/℃ | -164 | -88.6 | -0.5 | 熔点/℃ | 45 | 96 | 114 |
,
。
(2)COCl2俗称光气,分子中C原子采取 杂化成键;其中碳氧原子之间共价键含有
________(填字母):
a.2个σ键;b.2个π键;c.1个σ键.1个π键。
(3)金属是钛(22Ti) 将是继铜.铁.铝之后人类广泛使用的第四种金属,试回答:
I.Ti元素的基态原子的价电子层排布式为 ;
II.已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体,其组成均为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:a.分别取等质量的两种晶体的样品配成溶液;b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量发现产生的沉淀质量关系为:绿色晶体为紫色晶体的2/3。则绿色晶体配合物的化学式为 。
(18分)(1)I.短周期某主族元素M的电离能情况如右图(A)所示。则M元素位于周期表的第 族。
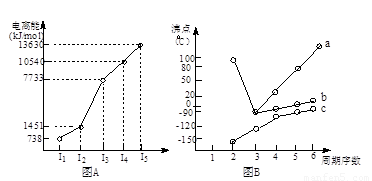
II.图B折线c可以表达出第 族元素氢化物的沸点的变化规律。两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线a和b,你认为正确的是:__________(填“a”或“b”)
III.部分有机物的熔沸点见下表:
|
烃 |
CH4 |
CH3CH3 |
CH3(CH2)2CH3 |
硝基苯酚 |
|
|
|
|
沸点/℃ |
-164 |
-88.6 |
-0.5 |
熔点/℃ |
45 |
96 |
114 |
根据物质结构理论,由这些数据你能得出的相关结论是(至少写2条):
,
。
(2)COCl2俗称光气,分子中C原子采取 杂化成键;其中碳氧原子之间共价键含有
________(填字母):
a.2个σ键;b.2个π键;c.1个σ键.1个π键。
(3)金属是钛(22Ti) 将是继铜.铁.铝之后人类广泛使用的第四种金属,试回答:
I.Ti元素的基态原子的价电子层排布式为 ;
II.已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体,其组成均为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:a.分别取等质量的两种晶体的样品配成溶液;b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量发现产生的沉淀质量关系为:绿色晶体为紫色晶体的2/3。则绿色晶体配合物的化学式为 。