题目内容
17.铁及其化合物是中学化学中的一类重要物质.下列关于铁元素的叙述中正确的是( )| A. | 2Fe3++Fe═3Fe2+成立说明氧化性:Fe3+>Fe2+ | |
| B. | 25℃、pH=0的溶液中,Al3+、NH4+、NO3-、Fe2+可以大量共存 | |
| C. | 5.6 g铁与足量的氯气反应失去的电子为0.2 mol | |
| D. | 硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H2O2+4H+═Fe3++4H2O |
分析 A.氧化剂的氧化性大于氧化产物的氧化性;
B.pH=0的溶液中存大大量的氢离子,H+、NO3-、Fe2+发生氧化还原反应;
C.氯气与铁反应生成氯化铁,1mol的铁转移3mol的电子;
D.电荷不守恒.
解答 解:A.2Fe3++Fe═3Fe2+反应中三价铁离子为氧化剂,二价铁离子为氧化产物,所以氧化性:Fe3+>Fe2+,故A正确;
B.pH=0的溶液中存大大量的氢离子,H+、NO3-、Fe2+发生氧化还原反应,三者不能大量共存,故B错误;
C.5.6 g铁的物质的量为0.1 mol与足量的氯气反应失去的电子为0.3 mol,故C错误;
D.硫酸亚铁溶液中加入过氧化氢溶液反应的离子方程式为:2Fe2++2H2O2+4H+=2Fe3++4H2O,故D错误;
故选:A.
点评 本题考查了元素化合物知识,明确铁及其化合物的性质是解题关键,注意C选项,氯气不足,转移电子数应依据氯气的量计算.

练习册系列答案
相关题目
5.反应4NH3+5O2?4NO+6H2O在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率表达正确的是( )
| A. | v(O2)=0.01 mol•(L•s)-1 | B. | v(NO)=0.008 mol•(L•s)-1 | ||
| C. | v(H2O)=0.003 mol•(L•s)-1 | D. | v(NH3)=0.003 mol•(L•s)-1 |
9.已知:CH4(g)+2O2(g)═CO2(g)+2H2O(1)△H1=-Q1 KJ/mol
2H2(g)+O2(g)═2H2O(g)△H2=-Q2 KJ/mol
2H2(g)+O2(g)═2H2O(1)△H3=-Q3KJ/mol
常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则下列说法正确的是( )
2H2(g)+O2(g)═2H2O(g)△H2=-Q2 KJ/mol
2H2(g)+O2(g)═2H2O(1)△H3=-Q3KJ/mol
常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则下列说法正确的是( )
| A. | 放出的热量为(0.4Q1+0.1Q3)KJ | B. | 放出的热量为(0.4Q1+0.05Q2)KJ | ||
| C. | 放出的热量为(0.4Q1+0.05Q3)KJ | D. | △H2<△H3 |
7.下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:①N,⑤Si,⑦C.
(2)画出原子的结构示意图:④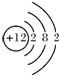 ,⑥
,⑥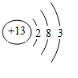 ,⑧
,⑧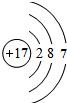 .
.
(3)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar.
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应: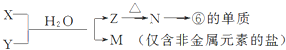
X溶液与Y溶液反应的离子方程式为Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$,
N→⑥的单质的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑,
(6)在③与④中,化学性质较活泼的是Na,怎样用化学实验证明?
答:与水反应;
在⑧与⑫中,化学性质较活泼的是Cl2,请用化学方程式来说明.
答:Cl2+2NaBr=2NaCl+Br2.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ⑬ | |||||||
| 2 | ① | ⑭ | ② | |||||
| 3 | ③ | ④ | ⑥ | ⑤ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)画出原子的结构示意图:④
 ,⑥
,⑥ ,⑧
,⑧ .
.(3)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar.
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
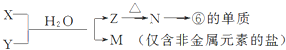
X溶液与Y溶液反应的离子方程式为Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$,
N→⑥的单质的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑,
(6)在③与④中,化学性质较活泼的是Na,怎样用化学实验证明?
答:与水反应;
在⑧与⑫中,化学性质较活泼的是Cl2,请用化学方程式来说明.
答:Cl2+2NaBr=2NaCl+Br2.
 固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1