题目内容
在8NH3+3Cl2=6NH4Cl+N2反应中,若有2mol N2生成,发生氧化反应的物质和该物质的量是
- A.16molNH3
- B.8molNH3
- C.4molNH3
- D.3molNH3
C
分析:在8NH3+3Cl2=6NH4Cl+N2反应中,氯气中氯元素化合价由0价降低为-1价,氯元素被还原,氨气中氮元素化合价由-3价升高为0价,氮元素被氧化,根据产物中氮元素化合价可知,参加反应的氨气中有 的起还原剂作用,
的起还原剂作用,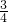 的氨气中氮元素化合价不变,仅作为反应物参加反应.据此解答.
的氨气中氮元素化合价不变,仅作为反应物参加反应.据此解答.
解答:在8NH3+3Cl2=6NH4Cl+N2反应中,氯气中氯元素化合价由0价降低为-1价,氯元素被还原,氨气中氮元素化合价由-3价升高为0价,氮元素被氧化,
根据产物中氮元素化合价可知,参加反应的氨气中有 的起还原剂作用,被氧化,
的起还原剂作用,被氧化,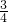 的氨气中氮元素化合价不变,仅作为反应物参加反应.
的氨气中氮元素化合价不变,仅作为反应物参加反应.
若有2molN2生成,由8NH3+3Cl2=6NH4Cl+N2反应可知,参加反应的氨气的总的物质的量为2mol×8=16mol,参加反应的氨气中有 的起还原剂作用,
的起还原剂作用,
所以被氧化的氨气为16mol× =4mol.故发生氧化的物质为氨气,其物质的量为4mol.
=4mol.故发生氧化的物质为氨气,其物质的量为4mol.
故选C.
点评:本题考查氧化还原反应概念及计算,难度不大,关键根据化合价变化判断参加反应的氨气中有 的起还原剂作用,可以根据氮元素化合价变化利用氮原子守恒计算起还原剂作用的氨气物质的量.
的起还原剂作用,可以根据氮元素化合价变化利用氮原子守恒计算起还原剂作用的氨气物质的量.
分析:在8NH3+3Cl2=6NH4Cl+N2反应中,氯气中氯元素化合价由0价降低为-1价,氯元素被还原,氨气中氮元素化合价由-3价升高为0价,氮元素被氧化,根据产物中氮元素化合价可知,参加反应的氨气中有
 的起还原剂作用,
的起还原剂作用,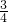 的氨气中氮元素化合价不变,仅作为反应物参加反应.据此解答.
的氨气中氮元素化合价不变,仅作为反应物参加反应.据此解答.解答:在8NH3+3Cl2=6NH4Cl+N2反应中,氯气中氯元素化合价由0价降低为-1价,氯元素被还原,氨气中氮元素化合价由-3价升高为0价,氮元素被氧化,
根据产物中氮元素化合价可知,参加反应的氨气中有
 的起还原剂作用,被氧化,
的起还原剂作用,被氧化,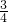 的氨气中氮元素化合价不变,仅作为反应物参加反应.
的氨气中氮元素化合价不变,仅作为反应物参加反应.若有2molN2生成,由8NH3+3Cl2=6NH4Cl+N2反应可知,参加反应的氨气的总的物质的量为2mol×8=16mol,参加反应的氨气中有
 的起还原剂作用,
的起还原剂作用,所以被氧化的氨气为16mol×
 =4mol.故发生氧化的物质为氨气,其物质的量为4mol.
=4mol.故发生氧化的物质为氨气,其物质的量为4mol.故选C.
点评:本题考查氧化还原反应概念及计算,难度不大,关键根据化合价变化判断参加反应的氨气中有
 的起还原剂作用,可以根据氮元素化合价变化利用氮原子守恒计算起还原剂作用的氨气物质的量.
的起还原剂作用,可以根据氮元素化合价变化利用氮原子守恒计算起还原剂作用的氨气物质的量. 
练习册系列答案
相关题目