题目内容
14.对下列现象或事实的解释正确的是( )| 选项 | 现象或事实 | 解释 |
| A | 用热的纯碱溶液洗去油污 | Na2CO3可直接与油污反应 |
| B | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
| C | 向Mg(OH)2悬浊液中滴加CuSO4溶液,生成蓝色沉淀 | Cu(OH)2的溶度积比Mg(OH)2的小,Mg(OH)2转化为Cu(OH)2 |
| D | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与NH4Cl反应会损失钾肥 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.热的纯碱溶液,促进碳酸根离子水解,碱性增强,碱性条件下油污水解为不可逆反应;
B.次氯酸钙与水、二氧化碳反应;
C.向Mg(OH)2悬浊液中滴加CuSO4溶液,生成蓝色沉淀,发生沉淀的转化;
D.K2CO3与NH4Cl相互促进水解生成氨气.
解答 解:A.热的纯碱溶液,促进碳酸根离子水解,碱性增强,碱性条件下油污水解为不可逆反应,解释不合理,故A错误;
B.次氯酸钙与水、二氧化碳反应,而氯化钙与二氧化碳不反应,解释不合理,故B错误;
C.向Mg(OH)2悬浊液中滴加CuSO4溶液,生成蓝色沉淀,发生沉淀的转化,则Cu(OH)2的溶度积比Mg(OH)2的小,故C正确;
D.K2CO3与NH4Cl相互促进水解生成氨气,不含损失钾肥,解释不合理,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握盐类水解、物质的性质、沉淀生成及转化、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
9.日常生活中常用到加碘食盐和铁强化酱油,这里的碘和铁指的是( )
| A. | 元素 | B. | 单质 | C. | 原子 | D. | 分子 |
5.已知弱酸等弱电解质电离时吸热.在测定中和热的实验中,下列说法正确的是( )
| A. | 为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触 | |
| B. | 使用环形玻璃搅拌棒是为了加大反应速率,减小实验误差 | |
| C. | 用0.5mol•L-1NaOH溶液分别与0.5 mol•L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同 | |
| D. | 在测定中和热实验中需要使用的仪器有:天平、量筒、烧杯、滴定管、温度计 |
2.实验室用稀硝酸与铜反应制备硝酸铜晶体及NO气体,需经过铜与稀硝酸反应、收集NO、尾气处理、制取硝酸铜晶体四个步骤,下列图示装置和原理能达到实验目的是( )
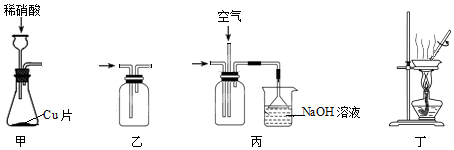

| A. | 用装置甲制取Cu(NO3)2和NO | B. | 用装置乙收集NO | ||
| C. | 用装置丙吸收尾气 | D. | 用装置丁蒸发结晶制Cu(NO3)2•3H2O |
9.下列各组离子在强酸性溶液中能大量共存的是( )
| A. | K+、Na+、HCO3-、SO42- | B. | Na+、Fe3+、I-、CI- | ||
| C. | Na+、NH4+、NO3-、CI- | D. | Na+、Ba2+、SO42-、NO3- |
19.晋代炼丹家、医学家葛洪所著《抱朴子》一书是中国为世界科技花园贡献出的一颗璀璨明珠,书中记载有“丹砂烧之成水银,积变又成丹砂”.这句话中的丹砂指的是HgS,下列关于这句话的说法正确的是( )
| A. | 这个过程只涉及物理变化 | |
| B. | 这个过程是可逆反应 | |
| C. | 这个过程发生了复分解反应 | |
| D. | “丹砂烧之成水银”过程中还可能产生SO2 |
6.下列图示装置的实验中,操作正确且能达到实验目的是( )
| A. |  如图:用食盐水制食盐晶体 | B. |  如图:分离碘酒中的碘和酒精 | ||
| C. |  如图:稀释浓硫酸 | D. | 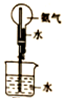 如图:验证氨水的碱性 |
3.下列措施不能加快Zn与1mol/LH2SO4反应产生H2的速率的是( )
| A. | 升高温度 | B. | 用Zn粉代替Zn粒 | ||
| C. | 滴加少量的CuSO4溶液 | D. | 改用0.1mol/LH2SO4与Zn反应 |