题目内容
将金属钠投入下列溶液中,没有沉淀生的是( )
| A、MgSO4溶液 |
| B、饱和NaHCO3溶液 |
| C、Ca(HCO3)2溶液 |
| D、饱和澄清石灰水 |
考点:钠的化学性质
专题:金属概论与碱元素
分析:钠和水反应生成氢氧化钠和氢气,再根据氢氧化钠和下列物质是否反应及生成物的溶解性判断.
解答:
解:A.钠和水反应生成氢氧化钠和氢气,氢氧化钠和硫酸镁发生复分解反应生成氢氧化镁沉淀,故A不符合;
B.钠和水反应生成氢氧化钠和氢气,氢氧化钠和碳酸氢钠反应生成碳酸钠和水,无沉淀生成,故B符合;
C.钠和水反应生成氢氧化钠和氢气,氢氧化钠和碳酸氢钙反应生成碳酸钙沉淀,故C不符合;
D.钠和水反应生成氢氧化钠和氢气,同时放出大量的热,温度升高,而氢氧化钙的溶解度随温度的升高而降低,故饱和石灰水有氢氧化钙沉淀产生,故D不符合;
故选B.
B.钠和水反应生成氢氧化钠和氢气,氢氧化钠和碳酸氢钠反应生成碳酸钠和水,无沉淀生成,故B符合;
C.钠和水反应生成氢氧化钠和氢气,氢氧化钠和碳酸氢钙反应生成碳酸钙沉淀,故C不符合;
D.钠和水反应生成氢氧化钠和氢气,同时放出大量的热,温度升高,而氢氧化钙的溶解度随温度的升高而降低,故饱和石灰水有氢氧化钙沉淀产生,故D不符合;
故选B.
点评:本题考查的是钠与碱、盐溶液的反应,实质就是钠先与水的反应.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
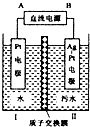 如图所示是利用电化学降解法治理水中的硝酸盐污染,电解槽中间用质子交换膜隔开,污水放入II区,通电使转NO3-化为N2,下面说法不正确的是( )
如图所示是利用电化学降解法治理水中的硝酸盐污染,电解槽中间用质子交换膜隔开,污水放入II区,通电使转NO3-化为N2,下面说法不正确的是( )| A、电解时H+从I区通过离子交换膜迁移到II区 |
| B、Ag-Pt电极上发生发应:2NO3-+10e-+6H2O═N2↑+12OH- |
| C、当电解过程中转移了1moL电子,则II区电解液质量减少2.8g |
| D、为增强溶液的导电性,I区水中可加入少量Na2SO4固体 |
下列说法正确的是( )
| A、含有共价键的物质一定是共价化合物 |
| B、只含有共价键的物质一定是共价化合物 |
| C、离子化合物中可能含有共价键 |
| D、氦分子中含有共价键 |
下列微粒中,哪一组中的化学键含有非极性共价键( )
①C2H6 ②H2S ③CH2Cl2 ④NH4+.
①C2H6 ②H2S ③CH2Cl2 ④NH4+.
| A、①②③④ | B、只有① |
| C、只有①③ | D、只有②③ |
同主族元素形成的同类型的化合物,往往其结构和性质相似.化合物PH4I是一种晶体,下列对它的叙述中不正确的是( )
| A、它是一种含有共价键的离子化合物 |
| B、这种化合物加热时,可能产生有色气体 |
| C、这种化合物中所有原子的最外层电子都达到了稳定结构 |
| D、这种化合物不能与强碱反应 |
下列反应的离子方程式正确的是( )
| A、向澄清石灰水中加入过量的二氧化碳:Ca2++2CO2+2OH-═Ca(HCO3)2 | ||||
B、在硫酸铁溶液中加入足量氢氧化钡溶液:Ba2++SO
| ||||
C、用足量氢氧化钠溶液吸收二氧化碳:2OH-+CO2═CO
| ||||
D、碳酸钠溶液与硫酸溶液反应:CO
|
实验室需配制一种仅含四种离子(不包括水电离的离子)的混合溶液,且在混合溶液中四种离子的物质的量浓度均为0.5mol/L,下列四个选项中能达到此目的是( )
| A、Fe2+ Na+ NO3- Cl- |
| B、Mg2+ NH4+ SO42- NO3- |
| C、H+ K+ Cl- CH3COO- |
| D、K+ NH4+ CO32- OH- |