题目内容
除去括号内杂质所用试剂或方法不正确的是( )
| 混合物 | 试剂 | 方法 | |
| A | Na2CO3固体(NaHCO3) | 无 | 加热 |
| B | NaBr溶液(NaI) | 溴水、CCl4 | 萃取、分液 |
| C | 酒精(水) | CaO | 蒸馏 |
| D | CO2(HCl) | 饱和Na2CO3溶液 | 洗气 |
| A、A | B、B | C、C | D、D |
考点:物质的分离、提纯的基本方法选择与应用
专题:实验评价题
分析:A.碳酸氢钠受热易分解;
B.溴与NaI反应生成NaBr和碘;
C.CaO与水反应后增大与乙醇的沸点差异;
D.二者均与饱和Na2CO3溶液反应.
B.溴与NaI反应生成NaBr和碘;
C.CaO与水反应后增大与乙醇的沸点差异;
D.二者均与饱和Na2CO3溶液反应.
解答:
解:A.碳酸氢钠受热易分解,则不需要试剂,加热即可除杂,故A正确;
B.溴与NaI反应生成NaBr和碘,则加溴水反应后、再加CCl4萃取、分液可除杂,故B正确;
C.CaO与水反应后增大与乙醇的沸点差异,然后蒸馏可除杂,故C正确;
D.二者均与饱和Na2CO3溶液反应,则洗气法不能除杂,应利用饱和NaHCO3溶液除杂,故D错误;
故选D.
B.溴与NaI反应生成NaBr和碘,则加溴水反应后、再加CCl4萃取、分液可除杂,故B正确;
C.CaO与水反应后增大与乙醇的沸点差异,然后蒸馏可除杂,故C正确;
D.二者均与饱和Na2CO3溶液反应,则洗气法不能除杂,应利用饱和NaHCO3溶液除杂,故D错误;
故选D.
点评:本题考查物质的分离、提纯的方法和应用,为高频考点,把握物质的性质及常见的混合物分离方法为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
在烧杯中加50mL水,将一小块金属钠投入烧杯中,产生现象:①钠浮在水面上②钠沉在水底③钠熔化成小球④小球迅速游动且逐渐减小⑤发出嘶嘶的声音⑥滴入酚酞后溶液不变色.上述有关描述正确的是( )
| A、②③⑤⑥ | B、全部 |
| C、①③④⑤ | D、③④⑤⑥ |
下列说法正确的是( )
| A、化合反应一定是放热反应 |
| B、分解反应一定是吸热反应 |
| C、在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
| D、破坏生成物全部化学键所需要的能量大于破坏反应物全部化学键所需要的能量时,反应为放热反应 |
下列叙述中正确的是( )
| A、元素电负性越大,元素第一电离能越大 |
| B、键能越大,键长越长,共价化合物越稳定 |
| C、副族元素中没有非金属元素 |
| D、离子化合物的熔点一定比共价化合物的高 |
实验是化学研究的基础.下列实验,不能达到实验目的是( )
A、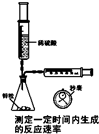 |
B、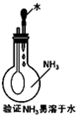 |
C、 |
D、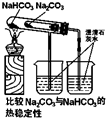 |
恒容容器中反应:A(g)+3B(g)?2C(g)+3D(g),达到平衡的标志是( )
①体系的压强不再改变
②混合气体的平均相对分子质量不再改变
③各组分的浓度不再改变
④混合气体的密度不变
⑤反应速率vA:vB:vC:vD=1:3:2:3
⑥单位时间内1mol A断键反应,同时2mol C也断键反应.
①体系的压强不再改变
②混合气体的平均相对分子质量不再改变
③各组分的浓度不再改变
④混合气体的密度不变
⑤反应速率vA:vB:vC:vD=1:3:2:3
⑥单位时间内1mol A断键反应,同时2mol C也断键反应.
| A、②③⑤⑥ | B、②③④⑤ |
| C、①④⑤⑥ | D、①②③⑥ |
将金属钠投入下列溶液中,没有沉淀生的是( )
| A、MgSO4溶液 |
| B、饱和NaHCO3溶液 |
| C、Ca(HCO3)2溶液 |
| D、饱和澄清石灰水 |
x、y为两种元素的原子,x的阴离子与y的阳离子具有相同的电子层结构,由此可知( )
| A、x的原子半径大于y的原子半径 |
| B、x的电负性小于y的电负性 |
| C、x的第一电离能大于y的第一电离能 |
| D、x的氧化性小于y的氧化性 |