题目内容
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3等杂质)中提取氧化铝的工艺流程如图:

请回答下列问题:
(1)操作Ⅰ、Ⅱ、Ⅲ的名称为 .
(2)检验溶液B中是否含有Fe3+,常用的试剂 (填化学式).
(3)不溶物A是 (填化学式),写出E→G反应的化学方程式 .写出D→E反应的化学方式 .
(4)说出溶液F中含碳元素溶质的一种用途 .

请回答下列问题:
(1)操作Ⅰ、Ⅱ、Ⅲ的名称为
(2)检验溶液B中是否含有Fe3+,常用的试剂
(3)不溶物A是
(4)说出溶液F中含碳元素溶质的一种用途
考点:物质分离和提纯的方法和基本操作综合应用,镁、铝的重要化合物,铁的氧化物和氢氧化物
专题:几种重要的金属及其化合物
分析:铝土矿的主要成分是Al2O3,含SiO2、Fe2O3等杂质,由流程可知,加足量盐酸过滤得到不溶物A为SiO2,溶液B中含Al3+、Fe3+,加过量NaOH溶液过滤得到不溶物B为Fe(OH)3,溶液D中含偏铝酸根离子,通入过量二氧化碳后过滤得到不溶物E为Al(OH)3,G为氧化铝,溶液F中含碳酸氢钠,以此来解答.
解答:
解:铝土矿的主要成分是Al2O3,含SiO2、Fe2O3等杂质,由流程可知,加足量盐酸过滤得到不溶物A为SiO2,溶液B中含Al3+、Fe3+,加过量NaOH溶液过滤得到不溶物B为Fe(OH)3,溶液D中含偏铝酸根离子,通入过量二氧化碳后过滤得到不溶物E为Al(OH)3,G为氧化铝,溶液F中含碳酸氢钠,
(1)由上述分析可知,操作Ⅰ、Ⅱ、Ⅲ的名称均为过滤,故答案为:过滤;
(2)检验溶液B中是否含有Fe3+,选KSCN溶液,若出现血红色,可证明含有,故答案为:KSCN溶液;
(3)由上述分析可知,A为SiO2,E→G反应的化学方程式为2Al(OH)3
Al2O3+3H2O,D→E反应的化学方式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,
故答案为:SiO2;2Al(OH)3
Al2O3+3H2O;NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3;
(4)溶液F中含碳酸氢钠,可作发酵粉或治疗胃酸的药物等,故答案为:作发酵粉或治疗胃酸的药物.
(1)由上述分析可知,操作Ⅰ、Ⅱ、Ⅲ的名称均为过滤,故答案为:过滤;
(2)检验溶液B中是否含有Fe3+,选KSCN溶液,若出现血红色,可证明含有,故答案为:KSCN溶液;
(3)由上述分析可知,A为SiO2,E→G反应的化学方程式为2Al(OH)3
| ||
故答案为:SiO2;2Al(OH)3
| ||
(4)溶液F中含碳酸氢钠,可作发酵粉或治疗胃酸的药物等,故答案为:作发酵粉或治疗胃酸的药物.
点评:本题考查物质的分离、提纯的方法及基本操作的综合应用,为高频考点,把握流程中物质的性质、发生的反应、混合物分离方法为解答的关键,侧重分析、推断及实验能力的综合考查,题目难度不大.

练习册系列答案
相关题目
某溶液中含有两种溶质NaCl和H2SO4,物质的量之比为3:1.用石墨作电极电解溶液,根据电极产物,可明显分为三个阶段.下列叙述不正确的是( )
| A、阴极只析出H2 |
| B、阳极先析出Cl2,后析出O2 |
| C、电解最后阶段为电解水 |
| D、溶液pH不断增大,最后为7 |
将一定质量的Mg,Zn,Al混合物与足量稀H2SO4反应,生成H22.8L(标准状况)原混合物的质量可能是( )
| A、2g | B、4g |
| C、7.8g | D、10g |
下列实验操作中正确的是( )
A、过滤时,如右图所示的装置进行操作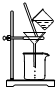 |
| B、蒸馏操作时,将温度计插入蒸馏烧瓶里的溶液中 |
| C、蒸发操作时,当混合物中的水分蒸干后停止加热 |
| D、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
硅及其化合物在材料领域中应用广泛.下列叙述不正确的是( )
| A、高纯度的硅单质广泛用于制作光导纤维 |
| B、传统无机非金属材料是指玻璃、水泥、陶瓷等硅酸盐材料 |
| C、二氧化硅是制造玻璃的主要原料 |
| D、自然界中硅元素贮量丰富 |

