题目内容
室温下,取0.2 mol·L-1CH3COOH溶液与0.2 mol·L-1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则下列说法(或关系式)正确的是 ( )
| A.混合溶液中由水电离出的c(H+)=10-8 mol·L-1 |
| B.溶液中离子浓度由大到小的顺序为c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| C.混合溶液中c(Na+)=c(CH3COOH)+c(CH3COO-)=0.2 mol·L-1 |
| D.混合溶液中c(OH-)-c(CH3COOH)=c(H+)=1×10-8 mol·L-1 |
D
解析

练习册系列答案
相关题目
现有常温下的五种溶液(如下表)。
| | ① | ② | ③ | ④ | ⑤ |
| 溶液 | 氨水 | 氢氧化钠 | 醋酸 | 盐酸 | 醋酸钠 |
| pH | 11 | 11 | 3 | 3 | 8.3 |
下列有关叙述中正确的是
A.五种溶液中,水电离出的c(OH-)最小的是⑤
B.将①、④两种溶液等体积混合,所得溶液中:c(Cl-) >c(NH4+)>c(H+)>c(OH-)
C.分别将①、②、③、④加水稀释100倍,稀释后四种溶液的pH:①>②>③>④
D.在⑤中加入适量的④至溶液呈中性,所得溶液中:c(Na+)>c(Cl-)=c(CH3COOH)
下列液体均处于25℃,下列有关叙述正确的是( )
| A.PH值相同的盐酸和氯化铵溶液中水的电离程度相同 |
| B.某溶液中由水电离出的c(H+)=10-13,则该溶液的PH一定为13 |
| C.PH=4.5的番茄汁中c(H+)是PH=6.5的牛奶中c(H+)的2倍 |
| D.中和浓度和体积均相同的盐酸和醋酸,消耗的氢氧化钠的物质的量之比为1:1 |
下列叙述正确的是 ( )
| A.一般认为沉淀离子浓度小于10-4 mol/L时,则认为已经沉淀完全 |
| B.反应AgCl+NaBr=AgBr+NaCl能在水溶液中进行,是因为AgBr比AgCl更难溶于水 |
C.Al(OH)3(s) Al3+(aq)+3OH-(aq)表示沉淀溶解平衡,Al(OH)3 Al3+(aq)+3OH-(aq)表示沉淀溶解平衡,Al(OH)3 Al3++3OH-表示水解平衡 Al3++3OH-表示水解平衡 |
| D.只有反应速率很高的化学反应才能应用于工业生产 |
把1 L 0.1 mol/L醋酸溶液用蒸馏水稀释到10 L,下列叙述正确的是 ( )
| A.c(CH3COOH)变为原来的1/10 |
| B.c(H+)变为原来的1/10 |
| C.c(CH3COO-)/c(CH3COOH)的比值增大 |
| D.溶液的导电性增强 |
50 ℃时,下列各溶液中,离子的物质的量浓度关系正确的是 ( )。
| A.pH=4的醋酸中:c(H+)=4.0 mol·L-1 |
| B.饱和小苏打溶液中:c(Na+)=c(HCO3—) |
| C.饱和食盐水中:c(Na+)+c(H+)=c(Cl-)+c(OH-) |
| D.pH=12的纯碱溶液中:c(OH-)=1.0×10-2 mol·L-1 |
在t°C时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如下图所示。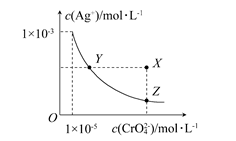
又知AgCl的Ksp=1.8×10-10。
下列说法不正确的是 ( )
| A.t°C时,Ag2CrO4的Ksp为1×10-8 |
| B.在饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点 |
| C.t°C时,Y点和Z点的Ag2CrO4的Ksp相等 |
| D.t°C时,将0.01 mol·L-1 AgNO3溶液滴入20 mL 0.01 mol·L-1 KCl和0.01 mol·L-1 K2CrO4的混合溶液中,Cl-先沉淀 |
欲同时对农作物施用含N、P、K三种元素的化肥,现有:①K2CO3、②KCl、③Ca(H2PO4)2、④(NH4)2SO4、⑤氨水,最适合的组合是( )。
| A.①②③ | B.②③④ | C.①③⑤ | D.②③⑤ |
