题目内容
4.下列有关化学用语表示正确的是( )| A. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | B. | 苯的结构简式:C6H6 | ||
| C. | 硅的原子结构示意图: | D. | Na2S的电子式: |
分析 A、中子数为20,则质量数为37,元素符号左上角的数字为质量数;
B、根据分子式和结构简式的特点来回答;
C、根据原子核外电子排布规律知识结合原子结构示意图的画法来回答分析;
D、硫化钠是钠离子和硫离子构成的离子化合物,根据离子化合物电子式的画法进行回答.
解答 解:A、中子数为20的氯原子中,质子数是17,但是质量数是37,中子数为20的氯原子为${\;}_{17}^{37}$Cl,故A错误;
B、苯的结构简式是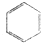 ,故B错误;
,故B错误;
C、硅是14号元素,它的原子结构示意图为: ,故C正确;
,故C正确;
D、硫化钠是钠离子和硫离子构成的离子化合物,Na2S的电子式是 ,故D错误;
,故D错误;
故选C.
点评 本题考查了电子式、化学式、结构简式的书写知识,题目难度中等,明确物质中存在的化学键及电子式的书写规则即可解答,注意离子键和共价键的区别,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
相关题目
15.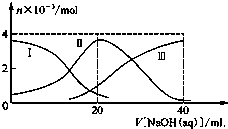 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )
 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )| A. | 当V[NaOH(aq)]=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| B. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大 | |
| C. | H2A第一步电离的方程式为H2A→HA-+H+ | |
| D. | 向NaHA溶液加入水稀释的过程中,pH可能增大也可能减少 |
12.下列实验不能达到目的是( )
| A. | 用分液的方法分离乙醇和乙酸 | |
| B. | 用NaOH溶液除去溴苯中的溴 | |
| C. | 用NaAlO2溶液和过量盐酸制备Al(OH)3 | |
| D. | 用足量铁粉除去FeCl2溶液中的FeCl3杂质 |
19.下列说法正确的是( )
| A. | 利用二氧化碳等原料合成的聚碳酸酯类可降解塑料替代聚乙烯塑料,可减少“白色污染” | |
| B. | 硅晶体的导电性介于导体与绝缘体之间,是一种重要的半导体材料,广泛应用于制造集成电路、光导纤维、太阳能电池板等 | |
| C. | pH计不能用于酸碱中和滴定终点的判断 | |
| D. | 2013年11月22日,中科院国家纳米科学中心宣布,该中心科研人员在国际上首次“拍”到氢键的“照片”,实现了氢键的实空间成像,为“氢键的本质”这一化学界争论了80多年的问题提供了直观证据.水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键 |
9.下列说法正确的是( )
| A. | 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)能自发进行,证明该反应的△H<0 | |
| B. | 常温下,BaSO4分别在相同物质的量浓度的Na2SO4溶液和Al2(SO4)3溶液中的溶解度相同 | |
| C. | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,说明常温下Ksp(BaCO3)<Ksp(BaSO4) | |
| D. | 等体积、等物质的量浓度的NH3•H2O溶液与NH4Cl溶液混合后溶液呈碱性,说明NH3•H2O的电离程度小于NH${\;}_{4}^{+}$的水解程度 |
16.常温下,下列各组离子在制定溶液中一定能大量共存的是( )
| A. | 使甲基橙变红色的溶液:Mg2+、Fe2+、SO42-、NO3- | |
| B. | 弱碱性溶液:Na+、Ca2+、HCO3-、NO3- | |
| C. | 使石蕊显紫色的溶液:Al3+、K+、SO42-、HCO3- | |
| D. | 0.1mol•L-1NaAlO2溶液:H+、Na+、Cl-、SO42- |
13.已知温度T时KW=1.0×10-12,0.1mol/L Na2A溶液pH=6,则下列说法中,正确的是( )
| A. | 该温度下,0.005mol/L H2A溶液中水电离出的c(H+)=10-12mol/L | |
| B. | H2A在水溶液中的电离方程式为:H2A?H++HA-,HA-?A2-+H+ | |
| C. | (NH4)2A溶液中存在离子浓度关系:(NH4+)>(A2-)>(H+)>(OH-) | |
| D. | 等体积等浓度的盐酸与H2A溶液分别与5.6gFe反应,H2A产生的H2多 |