题目内容
11.NA为阿伏加德罗常数,下列说法正确的是( )| A. | 标准状况下,11.2L的戊烷所含的分子数为0.5NA | |
| B. | 现有乙烯.丙烯.丁烯的混合气体共14g,其原子数为3NA | |
| C. | 1mol甲基(-CH3)所含的电子总数为7NA | |
| D. | 28g乙烯所含共用电子对数目为4NA |
分析 A.标准状况下,戊烷不是气体,不能使用标况下的气体摩尔体积计算戊烷的物质的量;
B.根据乙烯、丙烯和丁烯的最简式均为CH2来分析;
C.甲基不显电性,1个甲基电子数为9个;
D.求出乙烯的物质的量,然后根据1mol乙烯含6mol共用电子对来分析;
解答 解:A.标况下戊烷不是气体,不能使用标况下气体摩尔体积计算11.2L戊烷的物质的量,故A错误;
B.乙烯、丙烯和丁烯的最简式均为CH2,故14g混合气体中含有的CH2的物质的量n=$\frac{14g}{14g/mol}$=1mol,故含有3mol原子,故B正确;
C.甲基不显电性,故1mol甲基含9mol电子,故C错误;
D.28g乙烯的物质的量为1mol,而1mol乙烯含6mol共用电子对,故D错误;
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
15.某单官能团有机物的分子式为C3H8O,它可能的结构共有(不考虑立体异构)( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
2.探究Cu和浓硫酸的反应,下列装置或操作正确的是( )


| A. | 用装置甲、乙制备和收集SO2 | |
| B. | 用装置甲、丙制备和稀释CuSO4溶液 | |
| C. | 用装置乙、丁收集和检验SO2的漂白性 | |
| D. | 用装置甲、丁制备和探究SO2的漂白性 |
19.下列关于铝的叙述中,不正确的是( )
| A. | 铝是地壳里含量最多的金属元素 | B. | 铝容易失去电子,表现还原性 | ||
| C. | 在常温下,铝不能与氧气反应 | D. | 在空气中用酒精灯点不着 |
6.下列说法正确的是( )
| A. | 乙烯和聚乙烯均能使溴水褪色 | |
| B. | 苯可在FeBr3做催化剂时与溴水发生取代反应,从而使溴水褪色 | |
| C. | 乙酸和乙酸乙酯均能发生取代反应 | |
| D. | 天然橡胶、纤维素、动物油都是高分子化合物 |
16.下列有机物或有机物组合,在一定条件下不能发生聚合反应的是( )
| A. | 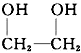 和HOOC-COOH 和HOOC-COOH | B. | HC≡CH | C. | 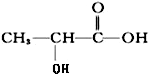 | D. | CH3COOH和C2H5OH |
20.第一位人工合成有机物的化学家是( )
| A. | 门捷列夫 | B. | 维勒 | C. | 拉瓦锡 | D. | 牛顿 |
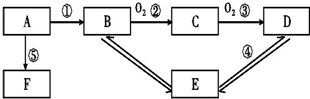
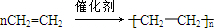 ;
;