��Ŀ����
���ᣨH3BO3����ʳƷ��ҽҩ����Ӧ�ù㷺��
��1�������B2H6������ˮ��Ӧ�Ļ�ѧ����ʽ��B2H6 + 6H2O=2H3BO3 +________��
��2��������������ͬʱ����ӦH3BO3+3CH3O HB(OCH3)3+3H2O�У�H3BO3��ת���ʣ�
HB(OCH3)3+3H2O�У�H3BO3��ת���ʣ� ���ڲ�ͬ�¶����淴Ӧʱ�䣨t���ı仯����ͼ���ɴ�ͼ�ɵó�
���ڲ�ͬ�¶����淴Ӧʱ�䣨t���ı仯����ͼ���ɴ�ͼ�ɵó�
��1�������B2H6������ˮ��Ӧ�Ļ�ѧ����ʽ��B2H6 + 6H2O=2H3BO3 +________��
��2��������������ͬʱ����ӦH3BO3+3CH3O
 HB(OCH3)3+3H2O�У�H3BO3��ת���ʣ�
HB(OCH3)3+3H2O�У�H3BO3��ת���ʣ� ���ڲ�ͬ�¶����淴Ӧʱ�䣨t���ı仯����ͼ���ɴ�ͼ�ɵó�
���ڲ�ͬ�¶����淴Ӧʱ�䣨t���ı仯����ͼ���ɴ�ͼ�ɵó�
���¶ȶ�Ӧ�÷�Ӧ�ķ�Ӧ���ʺ�ƽ���ƶ���Ӱ����_________________________
�ڸ÷�Ӧ�ġ�H_____0(�<������=����>��)��
��3��H3BO3��Һ�д������·�Ӧ��H3BO3(aq)+H2O(l) [B(OH)4]-(aq)+H+(aq)��֪0��70 mol��L-1
[B(OH)4]-(aq)+H+(aq)��֪0��70 mol��L-1
H3BO3��Һ�У�������Ӧ��298K�ﵽƽ��ʱ��cƽ����H+��=2�� 0 �� 10-5mol��L-1��cƽ����H3BO3����
c��ʼ��H3BO3����ˮ�ĵ���ɺ��Բ��ƣ�����¶��¸÷�Ӧ��ƽ�ⳣ��K��H2O��ƽ��Ũ�Ȳ�����K�ı���ʽ�У�������������λ��Ч���֣�
�ڸ÷�Ӧ�ġ�H_____0(�<������=����>��)��
��3��H3BO3��Һ�д������·�Ӧ��H3BO3(aq)+H2O(l)
 [B(OH)4]-(aq)+H+(aq)��֪0��70 mol��L-1
[B(OH)4]-(aq)+H+(aq)��֪0��70 mol��L-1 H3BO3��Һ�У�������Ӧ��298K�ﵽƽ��ʱ��cƽ����H+��=2�� 0 �� 10-5mol��L-1��cƽ����H3BO3����
c��ʼ��H3BO3����ˮ�ĵ���ɺ��Բ��ƣ�����¶��¸÷�Ӧ��ƽ�ⳣ��K��H2O��ƽ��Ũ�Ȳ�����K�ı���ʽ�У�������������λ��Ч���֣�
��1��6H2
��2���������¶ȣ���Ӧ���ʼӿ죬ƽ�������ƶ����ڣ�
��3�� ��1.43
��1.43
��2���������¶ȣ���Ӧ���ʼӿ죬ƽ�������ƶ����ڣ�
��3��
 ��1.43
��1.43 
��ϰ��ϵ�д�
 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�
�����Ŀ
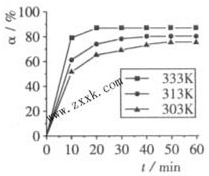 ��2010?�㶫�����ᣨH3BO3����ʳƷ��ҽҩ����Ӧ�ù㷺��
��2010?�㶫�����ᣨH3BO3����ʳƷ��ҽҩ����Ӧ�ù㷺�� B��OCH3��3+3H2O�У�H3BO3��ת���ʣ�a���ڲ�ͬ�¶����淴Ӧʱ�䣨t���ı仯��ͼ���ɴ�ͼ�ɵó���
B��OCH3��3+3H2O�У�H3BO3��ת���ʣ�a���ڲ�ͬ�¶����淴Ӧʱ�䣨t���ı仯��ͼ���ɴ�ͼ�ɵó��� [B��OH��4]-�� aq��+H+��aq����֪0.70mol?L-1 H3BO3��Һ�У�������Ӧ��298K�ﵽƽ��ʱ��cƽ����H+��=2.0��10-5mol?L-1��cƽ����H3BO3����c��ʼ��H3BO3����ˮ�ĵ���ɺ��Բ��ƣ�����¶��¸÷�Ӧ��ƽ�ⳣ��K��H2O��ƽ��Ũ�Ȳ�����K�ı���ʽ�У�������������λ��Ч���֣�
[B��OH��4]-�� aq��+H+��aq����֪0.70mol?L-1 H3BO3��Һ�У�������Ӧ��298K�ﵽƽ��ʱ��cƽ����H+��=2.0��10-5mol?L-1��cƽ����H3BO3����c��ʼ��H3BO3����ˮ�ĵ���ɺ��Բ��ƣ�����¶��¸÷�Ӧ��ƽ�ⳣ��K��H2O��ƽ��Ũ�Ȳ�����K�ı���ʽ�У�������������λ��Ч���֣�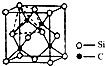 ��2013?��ɽ��ģ��̫���ܵ�صķ�չ�Ѿ������˵���������һ��Ϊ������̫���ܵ�أ��ڶ���Ϊ�ྦྷ�衢�Ǿ����̫���ܵ�أ�����������ͭ������CIGS��CIS�в���Ga���Ȼ����ﱡĤ̫���ܵ���Լ���ĤSiϵ̫���ܵ�أ�
��2013?��ɽ��ģ��̫���ܵ�صķ�չ�Ѿ������˵���������һ��Ϊ������̫���ܵ�أ��ڶ���Ϊ�ྦྷ�衢�Ǿ����̫���ܵ�أ�����������ͭ������CIGS��CIS�в���Ga���Ȼ����ﱡĤ̫���ܵ���Լ���ĤSiϵ̫���ܵ�أ�
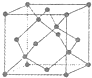 [��ѧ--ѡ�����ʽṹ������]Ŀǰ����ʡ������ڻ����ƹ�ʹ��̫���ܣ�������̫���ܵ���е�����̫���ܵ�ء��� ����̫���ܵ�ء�GaAs̫���ܵ�ؼ�ͭ��������Ĥ̫���ܵ�صȣ�
[��ѧ--ѡ�����ʽṹ������]Ŀǰ����ʡ������ڻ����ƹ�ʹ��̫���ܣ�������̫���ܵ���е�����̫���ܵ�ء��� ����̫���ܵ�ء�GaAs̫���ܵ�ؼ�ͭ��������Ĥ̫���ܵ�صȣ� _____0(�<������=����>��).
_____0(�<������=����>��). B(OCH3)3 +3H2O�У�H3BO 3��ת���ʣ�
B(OCH3)3 +3H2O�У�H3BO 3��ת���ʣ� ���ڲ�ͬ�¶����淴Ӧʱ�䣨t���ı仯��ͼ12���ɴ�ͼ�ɵó���
���ڲ�ͬ�¶����淴Ӧʱ�䣨t���ı仯��ͼ12���ɴ�ͼ�ɵó���
 _____0(�<������=����>��).
_____0(�<������=����>��).