题目内容
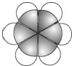
如图所示的装置,C、D、E、F、X、Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色.则以下说法正确的是( )


| A、电源B极是正极 |
| B、(甲)、(乙)装置的C、D、E、F电极均有单质生成,其物质的量比为1:2:2:2 |
| C、欲用(丙)装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液 |
| D、装置(丁)中X极附近红褐色不变 |
考点:电解原理
专题:电化学专题
分析:A、根据图片知,该装置是电解池,将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色,说明F极上氢离子放电生成氢气,所以F极是阴极,则电源B极是负极,A极是正极;
B、甲装置中C电极上氢氧根离子放电,D电极上铜离子放电,E电极上氯离子放电,F电极上氢离子放电,根据得失电子和生成物的关系式计算;
C、电镀时,镀层作阳极,镀件作阴极,电解质溶液中金属阳离子与阳极材料是相同的元素;
D、电解池中带正电荷的微粒向阴极移动,带负电荷的微粒向阳极移动.
B、甲装置中C电极上氢氧根离子放电,D电极上铜离子放电,E电极上氯离子放电,F电极上氢离子放电,根据得失电子和生成物的关系式计算;
C、电镀时,镀层作阳极,镀件作阴极,电解质溶液中金属阳离子与阳极材料是相同的元素;
D、电解池中带正电荷的微粒向阴极移动,带负电荷的微粒向阳极移动.
解答:
解:A、根据图片知,该装置是电解池,将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色,说明F极附近有大量氢氧根离子,由此得出F极上氢离子放电生成氢气,所以F极是阴极,则电源B极是负极,A极是正极,故A错误;
B、甲装置中C电极上氢氧根离子放电生成氧气,D电极上铜离子放电生成铜单质,E电极上氯离子放电生成氯气,F电极上氢离子放电生成氢气,所以(甲)、(乙)装置的C、D、E、F电极均有单质生成;生成1mol氧气需要4mol电子,生成1mol铜时需要2mol电子,生成1mol氯气时需要2mol电子,生成1mol氢气时需要2mol电子,所以转移相同物质的量的电子时生成单质的物质的量之比为1:2:2:2,故B正确;
C、若用(丙)装置给铜镀银,G应该是Ag,H是铜,电镀液是AgNO3溶液,故C错误;
D、丁装置中Y电极是阴极,氢氧化铁胶粒带正电荷,Y极附近红褐色变深,故D错误;
故选B.
B、甲装置中C电极上氢氧根离子放电生成氧气,D电极上铜离子放电生成铜单质,E电极上氯离子放电生成氯气,F电极上氢离子放电生成氢气,所以(甲)、(乙)装置的C、D、E、F电极均有单质生成;生成1mol氧气需要4mol电子,生成1mol铜时需要2mol电子,生成1mol氯气时需要2mol电子,生成1mol氢气时需要2mol电子,所以转移相同物质的量的电子时生成单质的物质的量之比为1:2:2:2,故B正确;
C、若用(丙)装置给铜镀银,G应该是Ag,H是铜,电镀液是AgNO3溶液,故C错误;
D、丁装置中Y电极是阴极,氢氧化铁胶粒带正电荷,Y极附近红褐色变深,故D错误;
故选B.
点评:本题考查了电解池原理,能正确判断电解池的阴阳极是解本题的关键,明确电泳现象证明了胶粒带电,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在一定条件下,将64g SO2气体和32g氧气通入密闭容器中生成SO3气体,达到平衡时,共放出热量78.64KJ,已知SO2在此条件下转化率为80%,则下列热化学方程式正确的是( )
A、SO2(g)+
| ||
| B、2SO2(g)+O2(g)?2SO3(g);△H=-196.6KJ?mol-1 | ||
C、SO2(g)+
| ||
| D、2SO2(g)+O2(g)?2SO3(g);△H=+196.6KJ?mol-1 |
将一块铁片放入500mL 1mol/L CuSO4溶液中,反应一段时间后,取出铁片,小心洗净后干燥称量,铁片增重0.8g,则反应后溶液中CuSO4的物质的量浓度是(反应前后溶液的体积不变)( )
| A、0.9mol/L |
| B、0.85mol/L |
| C、0.8mol/L |
| D、0.75mol/L |
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3.则下列说法正确的是( )
| A、反应过程中,被氧化与被还原的元素的物质的量之比为2:1 |
| B、NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉 |
| C、一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少空气污染 |
| D、若反应中生成1.0mol HNO3,转移的电子数目为6.02×1023 |
下列各组离子,可以在某澄清透明溶液中大量共存的是( )
| A、Mg2+、Cu2+、Cl-、SO42- |
| B、ClO-、Na+、H+、Cl- |
| C、Fe3+、H+、SO42-、I- |
| D、Na+、Ca2+、Cl-、HCO3- |
一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g)?Y(g)+Z(s),以下能说明作为反应达到平衡标志的是( )
| A、X的分解速率与Y的消耗速率相等 |
| B、X、Y、Z的物质的量比为2:1:1 |
| C、混合气体的密度不再变化 |
| D、单位时间内生成lmolY的同时分解2mol X |
下列物质中有顺反异构现象的是( )
| A、CH3-CH3 |
| B、H2C=CH2 |
C、 |
D、 |
 以下为五种有机物的有关信息,根据表中信息回答问题.
以下为五种有机物的有关信息,根据表中信息回答问题.