题目内容
苏合香醇可以用作食用香精,其结构简式如图1所示.
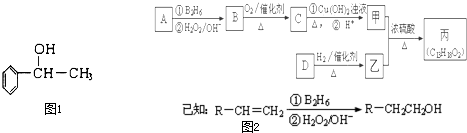
(一)(1)苏合香醇的分子式为 ,它不能发生的有机反应类型有(填数字序号) .
①取代反应 ②加成反应 ③消去反应 ④加聚反应 ⑤氧化反应 ⑥水解反应,
(二)有机物丙是一种香料,其合成路线如图2.其中甲的相对分子质量通过质谱法测得为88,它的核磁共振氢谱显示只有三组峰;乙与苏合香醇互为同系物.
(2)按照系统命名法,A的名称是 .
(3)C与新制Cu(OH)2悬浊液反应的化学方程式为 .
(4)丙中含有两个-CH3,D可发生银镜反应,在催化剂存在下1mol D与2mol H2可以反应生成乙,则D的结构简式为 .
(5)甲与乙反应的化学方程式为 .
(6)苯环上有3个取代基或官能团,且显弱酸性的乙的同分异构体共有 种,其中3个取代基或官能团互不相邻的有机物结构简式为 .

(一)(1)苏合香醇的分子式为
①取代反应 ②加成反应 ③消去反应 ④加聚反应 ⑤氧化反应 ⑥水解反应,
(二)有机物丙是一种香料,其合成路线如图2.其中甲的相对分子质量通过质谱法测得为88,它的核磁共振氢谱显示只有三组峰;乙与苏合香醇互为同系物.
(2)按照系统命名法,A的名称是
(3)C与新制Cu(OH)2悬浊液反应的化学方程式为
(4)丙中含有两个-CH3,D可发生银镜反应,在催化剂存在下1mol D与2mol H2可以反应生成乙,则D的结构简式为
(5)甲与乙反应的化学方程式为
(6)苯环上有3个取代基或官能团,且显弱酸性的乙的同分异构体共有
考点:有机物的推断
专题:有机物的化学性质及推断
分析:(一)苏合香醇为C6H5CH(OH)CH3,由-OH和苯环分析其性质;
(二)乙与苏合香醇互为同系物,乙为醇,则甲为羧酸,甲的相对分子质量通过质谱法测得为88,由丙的分子式可知,甲的分子式为C4H8O2,甲的核磁共振氢谱显示只有三组峰,则甲为2-甲基丙酸,结合合成转化图中的反应条件可知,A为2-甲基丙烯,B为2-甲基丙醇,C为2-甲基丙醛,甲与乙反应酯化生成丙(C13H18O2),则乙为C9H12O,(4)中丙中含有两个-CH3,D可发生银镜反应,在催化剂存在下1mol D与2mol H2可以反应生成乙,所以D为C9H8O,则D的结构简式为 ,乙为
,乙为 ,则丙为
,则丙为 ,据此解答.
,据此解答.
(二)乙与苏合香醇互为同系物,乙为醇,则甲为羧酸,甲的相对分子质量通过质谱法测得为88,由丙的分子式可知,甲的分子式为C4H8O2,甲的核磁共振氢谱显示只有三组峰,则甲为2-甲基丙酸,结合合成转化图中的反应条件可知,A为2-甲基丙烯,B为2-甲基丙醇,C为2-甲基丙醛,甲与乙反应酯化生成丙(C13H18O2),则乙为C9H12O,(4)中丙中含有两个-CH3,D可发生银镜反应,在催化剂存在下1mol D与2mol H2可以反应生成乙,所以D为C9H8O,则D的结构简式为
 ,乙为
,乙为 ,则丙为
,则丙为 ,据此解答.
,据此解答.解答:
解:(一)苏合香醇为C6H5CH(OH)CH3,由-OH和苯环可知,
(1)其分子式为C8H10O,能发生取代、加成、氧化、消去反应,而不能发生水解、加聚反应,
故答案为:C8H10O;④⑥;
(二)乙与苏合香醇互为同系物,乙为醇,则甲为羧酸,甲的相对分子质量通过质谱法测得为88,由丙的分子式可知,甲的分子式为C4H8O2,甲的核磁共振氢谱显示只有三组峰,则甲为2-甲基丙酸,结合合成转化图中的反应条件可知,A为2-甲基丙烯,B为2-甲基丙醇,C为2-甲基丙醛,甲与乙反应酯化生成丙(C13H18O2),则乙为C9H12O,(3)中丙中含有两个-CH3,D可发生银镜反应,在催化剂存在下1mol D与2mol H2可以反应生成乙,所以D为C9H8O,则D的结构简式为 ,乙为
,乙为 ,则丙为
,则丙为 ,
,
(2)由上述分析可知,A为2-甲基丙烯(或甲基丙烯),故答案为:2-甲基丙烯;
(3)C与新制Cu(OH)2悬浊液反应的化学方程式为:(CH3)2CHCHO+2Cu(OH)2
(CH3)2CHCOOH+Cu2O↓+2H2O,
故答案为:(CH3)2CHCHO+2Cu(OH)2
(CH3)2CHCOOH+Cu2O↓+2H2O;
(4)甲与乙反应酯化生成丙(C13H18O2),丙中含有两个-CH3,在催化剂存在下1molD与2molH2可以反应生成乙,D中不含甲基,所以D为D为C9H8O,则D的结构简式为 ,故答案为:
,故答案为: ;
;
(5)甲与乙反应的化学方程式为:(CH3)2CHCOOH+
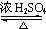
 +H2O,
+H2O,
故答案为:(CH3)2CHCOOH+
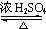
 +H2O;
+H2O;
(6)乙为C9H12O,结构简式为 ,其同分异构体符合:苯环上有3个取代基或官能团,显弱酸性,则侧链为-OH、-CH3、-CH2CH3,若-CH3、-CH2CH3相邻,-OH有4种位置,若若-CH3、-CH2CH3相间,-OH有4种位置,若若-CH3、-CH2CH3相对,-OH有2种位置,故共有10种,苯环上 3个取代基或官能团互不相邻,则该同分异构体为
,其同分异构体符合:苯环上有3个取代基或官能团,显弱酸性,则侧链为-OH、-CH3、-CH2CH3,若-CH3、-CH2CH3相邻,-OH有4种位置,若若-CH3、-CH2CH3相间,-OH有4种位置,若若-CH3、-CH2CH3相对,-OH有2种位置,故共有10种,苯环上 3个取代基或官能团互不相邻,则该同分异构体为 ,故答案为:10;
,故答案为:10; .
.
(1)其分子式为C8H10O,能发生取代、加成、氧化、消去反应,而不能发生水解、加聚反应,
故答案为:C8H10O;④⑥;
(二)乙与苏合香醇互为同系物,乙为醇,则甲为羧酸,甲的相对分子质量通过质谱法测得为88,由丙的分子式可知,甲的分子式为C4H8O2,甲的核磁共振氢谱显示只有三组峰,则甲为2-甲基丙酸,结合合成转化图中的反应条件可知,A为2-甲基丙烯,B为2-甲基丙醇,C为2-甲基丙醛,甲与乙反应酯化生成丙(C13H18O2),则乙为C9H12O,(3)中丙中含有两个-CH3,D可发生银镜反应,在催化剂存在下1mol D与2mol H2可以反应生成乙,所以D为C9H8O,则D的结构简式为
 ,乙为
,乙为 ,则丙为
,则丙为 ,
,(2)由上述分析可知,A为2-甲基丙烯(或甲基丙烯),故答案为:2-甲基丙烯;
(3)C与新制Cu(OH)2悬浊液反应的化学方程式为:(CH3)2CHCHO+2Cu(OH)2
| △ |
故答案为:(CH3)2CHCHO+2Cu(OH)2
| △ |
(4)甲与乙反应酯化生成丙(C13H18O2),丙中含有两个-CH3,在催化剂存在下1molD与2molH2可以反应生成乙,D中不含甲基,所以D为D为C9H8O,则D的结构简式为
 ,故答案为:
,故答案为: ;
;(5)甲与乙反应的化学方程式为:(CH3)2CHCOOH+

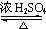
 +H2O,
+H2O,故答案为:(CH3)2CHCOOH+

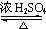
 +H2O;
+H2O;(6)乙为C9H12O,结构简式为
 ,其同分异构体符合:苯环上有3个取代基或官能团,显弱酸性,则侧链为-OH、-CH3、-CH2CH3,若-CH3、-CH2CH3相邻,-OH有4种位置,若若-CH3、-CH2CH3相间,-OH有4种位置,若若-CH3、-CH2CH3相对,-OH有2种位置,故共有10种,苯环上 3个取代基或官能团互不相邻,则该同分异构体为
,其同分异构体符合:苯环上有3个取代基或官能团,显弱酸性,则侧链为-OH、-CH3、-CH2CH3,若-CH3、-CH2CH3相邻,-OH有4种位置,若若-CH3、-CH2CH3相间,-OH有4种位置,若若-CH3、-CH2CH3相对,-OH有2种位置,故共有10种,苯环上 3个取代基或官能团互不相邻,则该同分异构体为 ,故答案为:10;
,故答案为:10; .
.
点评:本题考查有机物的推断,注意充分利用有机物的结构与分子式进行推断,熟练掌握官能团的性质与转化是解答本题的关键,题目难度中等.

练习册系列答案
相关题目
从节约原料和防止环境污染因素考虑,用铜制取硝酸铜,方法最佳的是( )
A、Cu
| |||||
B、Cu
| |||||
C、Cu
| |||||
D、Cu
|

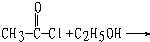
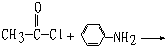
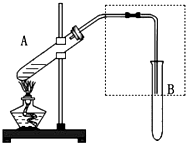 如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置.
如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置. 某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了O元素的非金属性比S强的实验研究.回答下列问题:
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了O元素的非金属性比S强的实验研究.回答下列问题: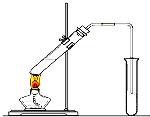 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: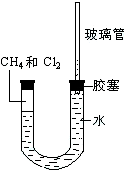 如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略.将该装置放置在有光亮的地方,让混和气体缓慢地反应一段时间.
如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略.将该装置放置在有光亮的地方,让混和气体缓慢地反应一段时间.