题目内容
 某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了O元素的非金属性比S强的实验研究.回答下列问题:
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了O元素的非金属性比S强的实验研究.回答下列问题:(1)图中D装置名称是
(2)N、C、Si的非金属性由强到弱的顺序是:
①稀HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
(3)①乙同学设计的实验所用到试剂A为
②写出C中发生反应的化学方程式
考点:性质实验方案的设计,实验装置综合
专题:实验设计题
分析:(1)根据装置图分析;
(2)根据同周期和同主族元素非金属性的变化规律分析;通过比较酸性强弱来判断非金属性强弱,装置中为强酸制备弱酸依此选择试剂;
(3)通过比较单质的氧化性来判断非金属性.
(2)根据同周期和同主族元素非金属性的变化规律分析;通过比较酸性强弱来判断非金属性强弱,装置中为强酸制备弱酸依此选择试剂;
(3)通过比较单质的氧化性来判断非金属性.
解答:
解:(1)由装置图可知,A为加液装置,A为分液漏斗,故答案为:长颈漏斗;
(2)同周期从左到右非金属性增强,则C<N,同主族元素从上到下非金属性:C>Si,所以非金属性由强到弱的顺序是:N>C>Si;通过比较酸性强弱来判断非金属性强弱,装置中为强酸制备弱酸,所以A中试剂为稀硝酸,B中为碳酸钙,C中为Na2SiO3溶液,
故答案为:N、C、Si; ①;④;
(3)①完成了O元素的非金属性比S强的实验研究,通过比较单质的氧化性来判断非金属性,所以用二氧化锰作催化剂使双氧水分解生成氧气,氧气通过氢硫酸或硫化钠溶液会生成硫单质,
故答案为:双氧水; 二氧化锰; 氢硫酸或硫化钠溶液;
②C中发生反应的方程式为:2H2S+O2=2S↓+2H2O,故答案为:2H2S+O2=2S+2H2O.
(2)同周期从左到右非金属性增强,则C<N,同主族元素从上到下非金属性:C>Si,所以非金属性由强到弱的顺序是:N>C>Si;通过比较酸性强弱来判断非金属性强弱,装置中为强酸制备弱酸,所以A中试剂为稀硝酸,B中为碳酸钙,C中为Na2SiO3溶液,
故答案为:N、C、Si; ①;④;
(3)①完成了O元素的非金属性比S强的实验研究,通过比较单质的氧化性来判断非金属性,所以用二氧化锰作催化剂使双氧水分解生成氧气,氧气通过氢硫酸或硫化钠溶液会生成硫单质,
故答案为:双氧水; 二氧化锰; 氢硫酸或硫化钠溶液;
②C中发生反应的方程式为:2H2S+O2=2S↓+2H2O,故答案为:2H2S+O2=2S+2H2O.
点评:本题考查了元素非金属性强弱的比较,为高频考点,侧重于考查学生的实验探究能力,注意把握物质的性质以及实验原理,题目难度中等.

练习册系列答案
相关题目
下列陈述ⅠⅡ正确并且有因果关系的是( )
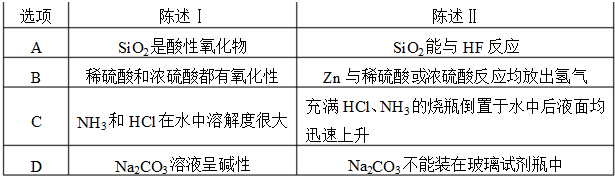

| A、A | B、B | C、C | D、D |
将铜片投入到稀硫酸中,铜片不溶,加入下列试剂后,可使铜片溶解的是( )
| A、稀盐酸 | B、硫酸钠晶体 |
| C、硝酸钠晶体 | D、氯化铁晶体 |
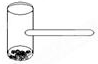 实验室里常用“碘锤”的玻璃仪器做碘的升华实验,该仪器为两头密封的玻璃窗,中间带有一根玻璃短柄.用此仪器进行有关实验时,具有装置简单、操作方便、现象明显、可反复使用等优点.用此仪器不能反复进行的实验是( )
实验室里常用“碘锤”的玻璃仪器做碘的升华实验,该仪器为两头密封的玻璃窗,中间带有一根玻璃短柄.用此仪器进行有关实验时,具有装置简单、操作方便、现象明显、可反复使用等优点.用此仪器不能反复进行的实验是( )| A、NH4Cl受热分解的实验 |
| B、无水CuSO4与胆矾的互变实验 |
| C、白磷和红磷(已经抽出O2)在一定温度下相互转变的实验 |
| D、KMnO4受热分解的实验 |
下列关于物质的检验说法正确的是( )
| A、加入氯化钡溶液有白色沉淀生成,再加稀硝酸,沉淀不消失,一定有硫酸根离子 |
| B、钾元素焰色反应的操作是:将铂丝放在稀盐酸中洗涤后灼烧至无色,然后再用铂丝蘸取固体氯化钾,进行灼烧,直接观察火焰颜色 |
| C、加入NaOH溶液,加热,放出能使湿润的红色石蕊试纸变蓝的气体,证明一定含有NH4+ |
| D、加入AgNO3溶液,有白色沉淀生成,证明含有Cl- |
如图所示与对应的叙述相符的是( )
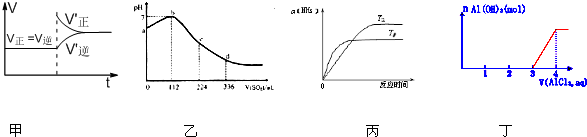

| A、甲图表示可逆反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2 (g)增大压强后,V正、V逆变化图 |
| B、乙图是标准状况下,某同学向100mL H2S饱和溶液中通入SO2,所得溶液pH变化图.由图可知ab段反应是:SO2+2H2S═3S↓+2H2O |
| C、丙图表明合成氨反应温度与转化率之间的关系,由图知合成氨反应是吸热反应 |
| D、丁图表明向一定量的NaOH溶液中逐滴加入AlCl3溶液的反应.说明反应分两步:①Al3++3OH-=Al(OH)3↓②Al(OH)3+OH-=AlO2-+2H2O |

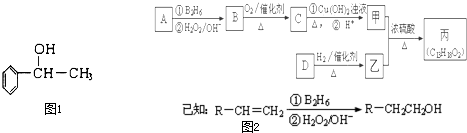
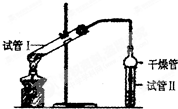 乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室制备乙酸乙酯的化学方程式如下:CH3COOH+C2H5OH
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室制备乙酸乙酯的化学方程式如下:CH3COOH+C2H5OH