题目内容
拟用图所示的装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去,必要时可以加热;a,b,c,d表示相应仪器加入的试剂).


上述方法中可以得到的干燥、纯净的气体是________.
(2)指出不能用上述方法制取的气体,说明理由(可以不填满)
①气体________,理由是________.
②气体________,理由是________.
③气体________,理由是________.
④气体________,理由是________.
答案:
解析:
提示:
解析:
|
答案:(1)NO (2)①C2H4 装置中没有温度计,无法控制反应温度 ②Cl2 反应生成的Cl2被(NaOH溶液)吸收了 ③NH3 反应生成的NH3被c(H2O)吸收了 |
提示:
|
该题考查实验室制取包括乙烯在内的常见气体的制取、净化、收集的原理和方法,考查实验设计与评价的能力. |

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
Ⅰ.某化学兴趣小组的同学用新制的氯水进行下列实验:①向氯水中滴入Na2CO3溶液;②向氯水中滴入AgNO3溶液;③向氯水中滴入紫色石蕊溶液.所观察到的实验现象如下,请将对应的实验序号填入下表空格中.
Ⅱ.该小组的同学为探究氨气的制取及其性质,进行了如下实验.
(1)在实验室中拟用下列方法制备氨气,其中不合理的是(填序号) .
A.加热浓氨水
B.将熟石灰和氯化铵的混合物加热
C.将浓氨水滴到生石灰上
D.加热氯化铵固体
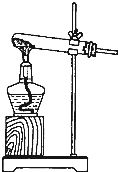
(2)根据上述正确的方法,选用图所示的装置制取氨气,写出试管中所发生反应的化学方程式 .一段时间后,将一端蘸有浓盐酸的玻璃棒接近导管口,观察到的现象是 ,该反应的化学方程式为 .
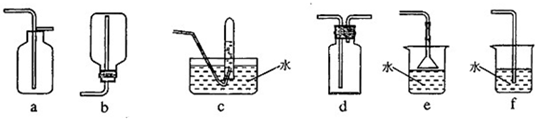
(3)同学们设计的收集、吸收氨气的几种装置如下图所示,其中能用于收集氨气的是(填序号) ;能用于吸收氨气尾气的是(填序号) .
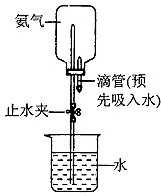
(4)将己收集满氨气的集气瓶,按图所示连接好装置(夹持装置己略去)进行喷泉实验时,请写出引发水上喷的操作是 .
| 实验序号 | 实验现象 |
| 溶液先变红后褪色 | |
| 有白色沉淀产生 | |
| 有气泡产生,氯水颜色变浅 |
(1)在实验室中拟用下列方法制备氨气,其中不合理的是(填序号)
A.加热浓氨水
B.将熟石灰和氯化铵的混合物加热
C.将浓氨水滴到生石灰上
D.加热氯化铵固体
(2)根据上述正确的方法,选用图所示的装置制取氨气,写出试管中所发生反应的化学方程式

(3)同学们设计的收集、吸收氨气的几种装置如下图所示,其中能用于收集氨气的是(填序号)

(4)将己收集满氨气的集气瓶,按图所示连接好装置(夹持装置己略去)进行喷泉实验时,请写出引发水上喷的操作是



