题目内容
(1)配制物质的量浓度为0.2mol/L NaOH溶液500mL,请回答下列问题:
应称量NaOH的质量 g,应选用容量瓶的规格 mL,除容量瓶外还需要的其它仪器,烧杯、玻璃棒、药匙 ,用托盘天平称取固体样品时(1g以下使用游码),若将样品放在了天平的右盘,读数为10.5g,则所称样品的实际质量为 g.
(2)下列操作对配制的NaOH溶液浓度有偏低影响的是 .
A.称量时将NaOH固体直接放在天平托盘上面的纸上
B.将称量的NaOH固体露置在空气的时间过长
C.选用的容量瓶内有少量的蒸馏水
D.在烧杯中溶解NaOH后,立即将所得溶液注入容量瓶中
E.整个配制过程中容量瓶不振荡.
应称量NaOH的质量
(2)下列操作对配制的NaOH溶液浓度有偏低影响的是
A.称量时将NaOH固体直接放在天平托盘上面的纸上
B.将称量的NaOH固体露置在空气的时间过长
C.选用的容量瓶内有少量的蒸馏水
D.在烧杯中溶解NaOH后,立即将所得溶液注入容量瓶中
E.整个配制过程中容量瓶不振荡.
考点:溶液的配制
专题:化学实验基本操作
分析:(1)根据m=cVM计算溶质的质量;选取容量瓶的规格应该等于或稍微大于需要配制溶液的体积;根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器;根据天平的使用方法是左物右码,左盘的质量等于右盘的质量加游码的质量,即药品质量=砝码质量+游码质量,如果位置放反,根据左盘的质量=右盘的质量+游码的质量,进行分析解答;
(2)根据c=
分析判断误差,如果n偏大或V偏小则配制溶液浓度偏高.
(2)根据c=
| n |
| V |
解答:
解:(1)NaOH的质量m=cVM=0.2mol/L×0.5L×40g/mol=4.0g;
选取容量瓶的规格应该等于或稍微大于需要配制溶液的体积,所以应该选取500mL的容量瓶;
溶液配制一般步骤是:计算→称量→溶解、冷却→移液→洗涤→定容→摇匀→装瓶贴签,一般用天平称量(用到药匙)称量,在烧杯中溶解,并用玻璃棒搅拌,冷却后转移到500mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,
由左盘的质量=右盘的质量+游码的质量可知:砝码质量=药品质量+游码的质量,若将样品放在了天平的右盘,药品质量=砝码质量-游码质量,故实际称量药品的质量=10g-0.5g=9.5g;
故答案为:4.0;500;托盘天平、胶头滴管;9.5;
(2)A.NaOH固体易潮解,称量时将NaOH固体直接放在天平托盘上面的纸上,NaOH固体的质量偏小,所配制溶液浓度偏小,故A正确;
B.将称量的NaOH固体露置在空气的时间过长,氢氧化钠会变质,NaOH固体的质量偏小,所配制溶液浓度偏小,故B正确;
C.选用的容量瓶内有少量的蒸馏水,对溶液的体积无影响,所配制溶液浓度不变,故C错误;
D.在烧杯中溶解NaOH后,立即将所得溶液注入容量瓶中,热溶液体积大,一旦冷却下来,溶液的体积偏小,所配制溶液浓度偏大,故C错误;
E.先加入的是密度较大的NaOH溶液,后加入的洗涤烧杯和玻璃棒的溶液密度较小,造成溶液密度不均匀,如果摇均匀密度大的和密度小的相溶体积会比二者原体积之和小,所配制溶液浓度偏大,故D错误;
故选AB.
选取容量瓶的规格应该等于或稍微大于需要配制溶液的体积,所以应该选取500mL的容量瓶;
溶液配制一般步骤是:计算→称量→溶解、冷却→移液→洗涤→定容→摇匀→装瓶贴签,一般用天平称量(用到药匙)称量,在烧杯中溶解,并用玻璃棒搅拌,冷却后转移到500mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,
由左盘的质量=右盘的质量+游码的质量可知:砝码质量=药品质量+游码的质量,若将样品放在了天平的右盘,药品质量=砝码质量-游码质量,故实际称量药品的质量=10g-0.5g=9.5g;
故答案为:4.0;500;托盘天平、胶头滴管;9.5;
(2)A.NaOH固体易潮解,称量时将NaOH固体直接放在天平托盘上面的纸上,NaOH固体的质量偏小,所配制溶液浓度偏小,故A正确;
B.将称量的NaOH固体露置在空气的时间过长,氢氧化钠会变质,NaOH固体的质量偏小,所配制溶液浓度偏小,故B正确;
C.选用的容量瓶内有少量的蒸馏水,对溶液的体积无影响,所配制溶液浓度不变,故C错误;
D.在烧杯中溶解NaOH后,立即将所得溶液注入容量瓶中,热溶液体积大,一旦冷却下来,溶液的体积偏小,所配制溶液浓度偏大,故C错误;
E.先加入的是密度较大的NaOH溶液,后加入的洗涤烧杯和玻璃棒的溶液密度较小,造成溶液密度不均匀,如果摇均匀密度大的和密度小的相溶体积会比二者原体积之和小,所配制溶液浓度偏大,故D错误;
故选AB.
点评:本题考查一定物质的量浓度溶液的配制,难度不大,注意容量瓶规格的选取方法、误差的判断方法为易错点.

练习册系列答案
相关题目
化学与生活、社会密切相关.下列说法不正确的是( )
| A、少开汽车可一定程度地减缓雾霾现象 |
| B、为提高作物产量大量使用农药和化肥 |
| C、使用无磷洗衣粉能缓解水体富营养化 |
| D、合理利用可燃冰有利于弥补能源短缺 |
下列说法不正确的是( )
| A、做“钠与水的反应”实验时,切取绿豆大小的金属钠,用滤纸吸干其表面的煤油,放入烧杯中,滴入两滴酚酞溶液,再加入少量水,然后观察并记录实验现象 |
| B、单晶硅是将太阳能转变为电能的常用材料 |
| C、二氧化硫、氮氧化物、总悬浮颗粒物属于大气监测,空气质量日报的内容 |
| D、一旦金属汞洒落,必须尽可能收集起来,放在水中保存以防挥发;并将硫磺粉撒在洒落的地方,使金属汞转变成不挥发的硫化汞 |


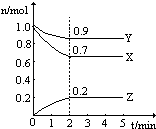 温度一定,在一个10L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.试根据图中数据,填写下列空白:
温度一定,在一个10L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.试根据图中数据,填写下列空白: