题目内容
下列叙述正确的是
A.0.1mol·L-1CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
B.NH4Cl溶液加水稀释后,恢复至原温度,pH和KW均增大
C.pH=4的CH3COOH溶液和pH=4的NH4Cl溶液中,c(H+)不相等
D.在NaHCO3溶液中:c(OH-)+c(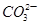 )=c(H+)+c(H2CO3)
)=c(H+)+c(H2CO3)
【答案】
D
【解析】
试题分析:A、0.1mol·L-1CH3COONa溶液中离子浓度关系为:c(CH3COO-)>c(Na+)>c(OH-)>c(H+),错误;B、NH4Cl溶液加水稀释后,恢复至原温度,pH增大,但温度不变,KW不变,错误;C、pH=4的CH3COOH溶液和pH=4的NH4Cl溶液中,c(H+)相等,均为10—4 mol·L-1,错误;D、联立NaHCO3溶液中的电荷守恒式和物料守恒式知,c(OH-)+c(CO32—)=c(H+)+c(H2CO3),正确。
考点:考查电解质溶液中离子浓度关系和三个守恒式。

练习册系列答案
相关题目
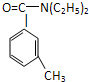 避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH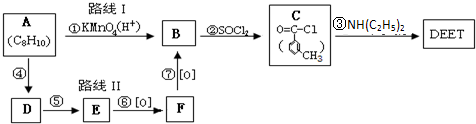
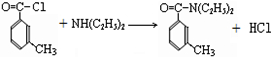
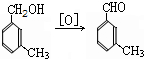
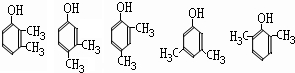 (任写2种)
(任写2种)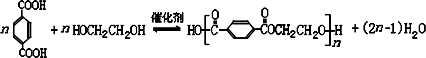
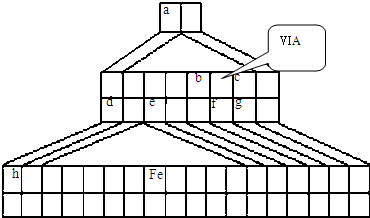
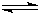 NH3?H2O+H+
NH3?H2O+H+ (2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
(2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.