题目内容
7.某物质中可能有甲酸、乙酸、甲醇和甲酸乙酯四种物质中的一种或几种.在鉴定时有下列现象:①有银镜反应;②加入新制的Cu(OH)2 悬浊液后未发现变澄清;③与含酚酞的NaOH溶液共热,红色逐渐消失.下列结论正确的是( )| A. | 有甲酸乙酯,可能有甲醇 | B. | 有甲酸乙酯和甲酸 | ||
| C. | 有甲酸乙酯和甲醇 | D. | 几种物质均存在 |
分析 ①有银镜反应;说明分子结构中含有醛基;
②加入新制氢氧化铜悬浊液少许,未发现变澄清,沉淀不溶解,说明不含羧酸;
③与含酚酞的氢氧化钠溶液共热,红色逐渐消失,说明和氢氧化钠反应.
解答 解:①有银镜反应,说明分子结构中含有醛基,含甲酸或甲酸乙酯或都有;
②加入新制氢氧化铜悬浊液少许,未发现变澄清,沉淀不溶解,则说明不含羧酸,则没有甲酸;
③与含酚酞的氢氧化钠溶液共热,红色逐渐消失,说明和氢氧化钠反应,而醇、醛不与NaOH反应,
则一定含有甲酸乙酯,一定不存在甲酸,可能有甲醇,
故选A.
点评 本题考查了有机物的鉴别,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握分子结构中官能团的特征性质是解题关键,熟悉醛、酯的性质即可解答,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.下列有关叙述正确的是( )
| A. | 元素的化学性质随着相对原子质量的递增而呈周期性变化 | |
| B. | 元素周期律的实质是因为元素原子最外层电子数由1→8周期性变化而引起的 | |
| C. | 半径由大到小、氧化性由弱到强的是K+、Mg2+、Al3+、H+,而还原性由弱到强的则是I-、Br-、Cl-、F- | |
| D. | 某元素R的最高价氧化物化学式为R2O5,又知R的气态氢化物中含氢的质量分数为8.8%,则R的相对原子质量为28 |
18.下列物质互为同分异构体的一组是( )
| A. | 12C和14C | B. | O2和O3 | ||
| C. | CH3CH2OH和CH3OCH3 | D. |  和 和  |
15.历史上最早应用的还原性染料--靛蓝,其结构简式如图所示,下列关于靛蓝的叙述中不正确的是( )


| A. | 该物质是高分子化合物 | B. | 它的分子式是C15H10N2O2 | ||
| C. | 靛蓝由碳、氢、氧、氮四种元素组成 | D. | 它是不饱和的有机物 |
19.下列说法正确的是( )
| A. | SiH4比CH4稳定 | |
| B. | O2-半径比F-的小 | |
| C. | Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 | |
| D. | 酸性 HClO4>H2SO4>CH3COOH>H2CO3 |
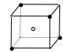 A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A、D同主族,E和其它元素既不同期也不同主族,B、C、D最高价氧化物的水化物两两混合均能发生反应,A和E可组成离子化合物,其晶体结构示意图如图所示,其中“●”代表阳离子,“○”代表阴离子.
A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A、D同主族,E和其它元素既不同期也不同主族,B、C、D最高价氧化物的水化物两两混合均能发生反应,A和E可组成离子化合物,其晶体结构示意图如图所示,其中“●”代表阳离子,“○”代表阴离子. H++F-.
H++F-.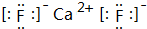 ,其晶体类型为离子晶体.
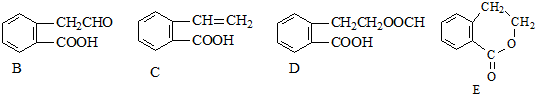
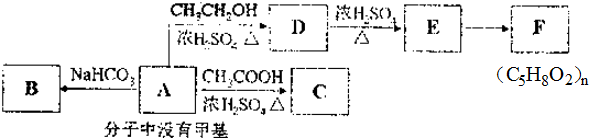
,其晶体类型为离子晶体. ,它可通过不同化学反应分别制得如图B、C、D和E四种物质.
,它可通过不同化学反应分别制得如图B、C、D和E四种物质. ,反应类型:氧化反应
,反应类型:氧化反应 +H2O,反应类型:酯化反应或取代反应
+H2O,反应类型:酯化反应或取代反应 .
.
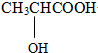 .
.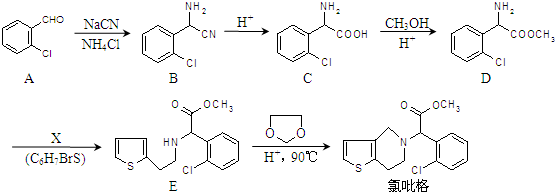
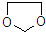 在酸性条件下生成氯吡格雷和另一种常见有机物,该有机物在浓硫酸催化下,加热脱水生成乙炔,试写出该有机物脱水生成乙炔的方程式.CH2OHCH2OH$→_{△}^{浓H_{2}SO_{4}}$CH≡CH↑+2H2O
在酸性条件下生成氯吡格雷和另一种常见有机物,该有机物在浓硫酸催化下,加热脱水生成乙炔,试写出该有机物脱水生成乙炔的方程式.CH2OHCH2OH$→_{△}^{浓H_{2}SO_{4}}$CH≡CH↑+2H2O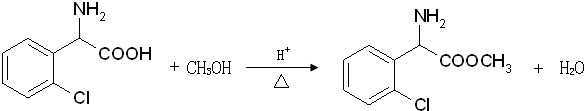
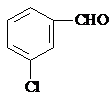 、
、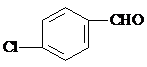 、
、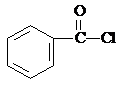 .
.