题目内容
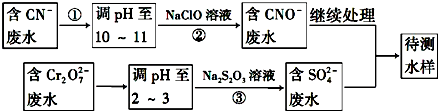
2.为了除去粗盐中的Ca2+、Mg2+、SO${\;}_{4}^{2-}$及泥沙,可将粗盐溶于水,然后进行下列5项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液.正确的操作顺序可以是( )| A. | ⑤②④③① | B. | ④①②⑤③ | C. | ②⑤④①③ | D. | ①④②⑤③ |
分析 除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可以加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除钙离子和过量的钡离子.盐酸要放在最后,来除去过量的氢氧化钠和碳酸钠,加氢氧化钠和氯化钡无先后顺序要求.
解答 解:泥沙可用过滤除掉,镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,蒸发除掉水和过量的氯化氢,所以正确的顺序为:⑤加过量的BaCl2溶液,④加过量的Na2CO3溶液,②加过量的NaOH溶液,①过滤,③加适量的盐酸;(或者②加过量的NaOH溶液,⑤加过量的BaCl2溶液,④加过量的Na2CO3溶液,①过滤,③加适量的盐酸).所以正确的顺序是⑤④②①③或②⑤④①③.
故选C.
点评 本题主要考查了除杂质的原则,以及除杂质的顺序,题目难度不大,注意为了将杂质除净,每次所加试剂要过量,侧重于考查学生的分析能力.

练习册系列答案
相关题目
15.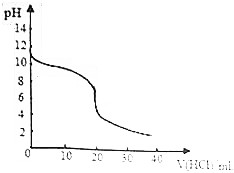 常温下,向20.00mL0.1000mol/L的氨水中逐滴加入0.1000mol/L的盐酸,pH随盐酸体积的变化如图所示.下列说法正确的是( )
常温下,向20.00mL0.1000mol/L的氨水中逐滴加入0.1000mol/L的盐酸,pH随盐酸体积的变化如图所示.下列说法正确的是( )
 常温下,向20.00mL0.1000mol/L的氨水中逐滴加入0.1000mol/L的盐酸,pH随盐酸体积的变化如图所示.下列说法正确的是( )
常温下,向20.00mL0.1000mol/L的氨水中逐滴加入0.1000mol/L的盐酸,pH随盐酸体积的变化如图所示.下列说法正确的是( )| A. | 滴加盐酸10mL 时,c(Cl-)>c(NH4+)>c(NH3•H2O)>c(OH-)>c(H+) | |
| B. | 滴加盐酸20m时,c(H+)=c(OH-)+c(NH3•H2O) | |
| C. | 滴加盐酸10 mL时溶液的导电能力与滴加盐酸20mL时溶液的导电能力相同 | |
| D. | pH<7时,消耗盐酸的体积一定大于20.00mL |
16.关于化学键的下列叙述中正确的是( )
| A. | 离子化合物可能含共价键 | B. | 共价化合物可能含离子键 | ||
| C. | 离子化合物中只含离子键 | D. | 离子化合物一定不含共价键 |
13.几种有机化合物的结构简式如下:①CH3-CHO;②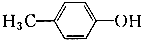 ;③
;③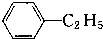 ;④CH3COOC2H5;⑤
;④CH3COOC2H5;⑤ ;⑥
;⑥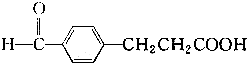 ,有关上述有机化合物的类别叙述正确的是( )
,有关上述有机化合物的类别叙述正确的是( )
 ;③
;③ ;④CH3COOC2H5;⑤
;④CH3COOC2H5;⑤ ;⑥
;⑥ ,有关上述有机化合物的类别叙述正确的是( )
,有关上述有机化合物的类别叙述正确的是( )| A. | ①醛,②酚,③环烷烃,④酯,⑤羧酸,⑥酯 | |
| B. | ①醇,②酚,③芳香烃,④酚,⑤芳香烃,⑥羧酸 | |
| C. | ①醛,②醇,③芳香烃,④羧酸,⑤羧酸,⑥醛 | |
| D. | ①醛,②酚,③芳香烃,④酯,⑤羧酸,⑥羧酸 |
20.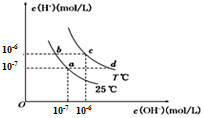 在不同温度下,水溶液中c(H+)与c(OH- )有如图所示关系.下列说法正确的是( )
在不同温度下,水溶液中c(H+)与c(OH- )有如图所示关系.下列说法正确的是( )
 在不同温度下,水溶液中c(H+)与c(OH- )有如图所示关系.下列说法正确的是( )
在不同温度下,水溶液中c(H+)与c(OH- )有如图所示关系.下列说法正确的是( )| A. | c点对应的溶液pH=6,溶液呈弱酸性 | |
| B. | b点对应的溶液中可以大量共存:NH4+、K+、CO32-、Cl- | |
| C. | 若a点表示CH3COOH和CH3COONa的混合溶液,则该溶液中的离子浓度大小为:c(Na+ )>c(CH3COO-)>C(OH- )>c(H + ) | |
| D. | 若d点表示某等浓度、等体积的NH3•H2O和NH4Cl混合溶液,则溶液中的离子浓度存在如下关系:c(NH4+)+2c(H+)═2c(OH-)+c(NH3•H2O) |
11.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ•mol-1
②CH3OH(g)+O2(g)═CO2(g)+2H2(g)△H=-192.9kJ•mol-1
下列说法正确的是( )
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ•mol-1
②CH3OH(g)+O2(g)═CO2(g)+2H2(g)△H=-192.9kJ•mol-1
下列说法正确的是( )
| A. | CH3OH的燃烧热(△H)为-192.9kJ•mol-1 | |
| B. | 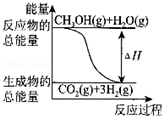 反应①中的能量变化如图所示 | |
| C. | CH3OH转变成H2的过程一定要吸收能量 | |
| D. | 根据②推知反应:CH3OH(l)+O2(g)═CO2(g)+2H2(g)的△H>-192.9kJ•mol-1 |
12.下列离子方程式中正确的是( )
| A. | 氯气溶于水中:Cl2+H2O=2H++Cl-+ClO- | |
| B. | 硫酸氢钠溶液与氢氧化钡溶液混合至混合液呈中性:2HSO4-+Ba2++2OH-=BaSO4↓+2H2O+SO42- | |
| C. | 向双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O | |
| D. | 用铜作阳极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ |
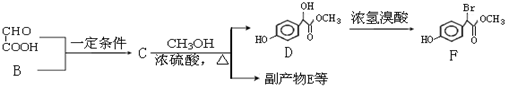
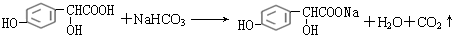 .
. .
.