题目内容
8. 汽车排气中的CO、NOX已经成为大气的主要污染物,使用稀土等催化剂能将CO、NOx、碳氢化合物转化成无毒物质,从而减少汽车尾气污染.
汽车排气中的CO、NOX已经成为大气的主要污染物,使用稀土等催化剂能将CO、NOx、碳氢化合物转化成无毒物质,从而减少汽车尾气污染.(1)已知:
N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol
2C(s)+O2(g)═2CO(g)△H=-221.0kJ/mol
C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
试写出NO与CO催化转化成N2和CO2的热化学方程式:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-746.5kJ/mol
(2)在容积相同的两个密闭容器内(装有等量的某种催化剂),分别充入同量的NOx及C3H6,在不同温度下,同时发生以下反应:
18NO(g)+2C3H6(g)?9N2(g)+6CO2(g)+6H2O(g);
18NO2(g)+4C3H6(g)?9N2(g)+12CO2(g)+12H2O(g);
并分别在t秒时测定其中NOx转化率,绘得图象如图所示:
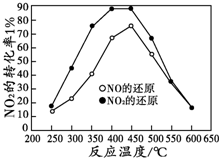
①从图中可以得出的结论是
结论一:从测定NOX转化数据中判断,相同温度下NO转化效率比NO2的低
结论二:在250°C-450°C时,NOx转化率随温度升高而增大,450°C-600°C时NOx转化率随温度升高而减小
②在上述NO2和C3H6反应中,提高NO2转化率的措施有BC.(填编号)
A.加入催化剂 B.降低温度 C.分离出H2O(g) D.增大压强
(3)CO的中毒是由于CO与血液中血红蛋白的血红素部分反应生成碳氧血红蛋白(Hb•CO),在37℃时:CO+Hb•O2?O2+Hb•CO K=220
实验表明,Hb•CO的浓度即使只有Hb•O2浓度的2%,也可造成人的智力损伤.抽烟后,测得平衡时人体肺部的空气中CO和O2的浓度分别为10-6mol•L-1和10-2mol•L-1.请问,抽烟会造成人的智力损伤吗?(写出计算过程)
分析 (1)根据方程式的加减得出NO与CO催化转化成N2和CO2的化学方程式,焓变相应的加减,从而得出其热化学反应方程式;
(2)①根据图象分析;
②根据外界条件对化学平衡的影响分析;
(3)根据化学平衡常数计算Hb•CO的浓度与Hb•O2的浓度的比值与2%比较判断.
解答 解:(1)N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol①
2C(s)+O2(g)=2CO(g)△H=-221.0kJ/mol②
C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol ③
方程式③×2-②-①得NO (g)+2CO(g)=N2(g)+2CO2(g)
所以△H=(-393.5kJ/mol)×2-(-221.0kJ/mol)-(+180.5kJ/mol)=-746.5 kJ/mol,
故答案为:2NO (g)+2CO(g)=N2(g)+2CO2(g)△H=-746.5 kJ/mol;
(2)①通过图象知,NO转化效率比NO2 的低;在250°C-450°C时,NOx转化率随温度升高而增大,450°C-600°C时NOx转化率随温度升高而减小.
故答案为:NO转化效率比NO2 的低;在250°C-450°C时,NOx转化率随温度升高而增大,450°C-600°C时NOx转化率随温度升高而减小;
②根据图象知,温度越高(450度),二氧化氮的转化率越小,所以该反应是放热反应,且该反应是气体体积增大的反应.
A、催化剂只改变反应到达平衡的时间,不改变化学平衡状态,故A错误;
B、该反应是放热反应,所以降低温度,平衡向正反应方向移动,增大二氧化氮的转化率,故B正确;
C、分离出H2O(g),减少生成物的浓度,平衡向正反应方向移动,增大二氧化氮的转化率,故C正确;
D、该反应是气体体积增大的反应,增大压强,平衡向逆反应方向移动,二氧化氮的转化率降低,故D错误;
故答案为:BC;
(3)肺部CO和O2的浓度分别为10-6mol•L-1和10-2mol•L-1,K=$\frac{c(Hb•CO)•c({O}_{2})}{c(Hb•{O}_{2})•c(CO)}$=$\frac{c(Hb•CO)×1{0}^{-2}}{c(Hb•{O}_{2})×1{0}^{-6}}$=220,$\frac{C(Hb•CO)}{C(Hb•{O}_{2})}×100%$=2.2%>2%,
答:抽烟会造成人的智力损伤.
点评 本题考查了盖斯定律、外界条件对化学平衡的影响等知识点,难度不大,注意盖斯定律的应用时,方程式加减,焓变也应相应的加减.

| 选项 | 含杂质的物质 | 试剂 | 除杂方法 |
| A | C2H4(SO2) | NaOH溶液 | 洗气 |
| B | C6H6(苯酚) | 浓Br2水 | 过滤 |
| C | C6H5NO2(HNO3) | NaOH溶液 | 分液 |
| D | C2H2(H2S) | CuSO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
[实验设计]控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验.
(1)请完成以下实验设计表(表中不要留空格).
| 实验编号 | 实验目的 | T/K | pH | c/10-3mol•L-1 | |
| H2O2 | Fe2+ | ||||
| ① | 为以下实验作参考 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 | ||||
| ③ | 298 | 10 | 6.0 | 0.30 | |
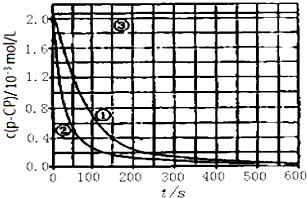
(2)请根据如图实验①曲线,计算降解反应在50-150s内的反应速率:v(p-CP)=8.0×10-6mol/(L•s).
[解释与结论]
(3)实验①、②表明温度升高,降解反应速率增大.但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:过氧化氢在温度过高时迅速分解.
(4)实验③得出的结论是:pH等于10时,反应速率趋向于零(或该降解反应趋于停止).
(5)根据题意:在一定条件下H2O2和Fe2+的离子反应式H2O2+2H++2Fe2+=2H2O+2Fe3+.
| A. | NaCl(aq)$\stackrel{CO_{2}}{→}$NaHCO3(s) $\stackrel{△}{→}$Na2CO3(s) | |
| B. | CuCl2$\stackrel{NaOH(aq)}{→}$ Cu(OH)2 $→_{△}^{葡萄糖}$Cu | |
| C. | Al $\stackrel{NaOH(aq)}{→}$ NaAlO2(aq) $\stackrel{△}{→}$ NaAlO2(s) | |
| D. | MgO(s)$\stackrel{HNO_{3}(aq)}{→}$ Mg(NO3)2(aq) $\stackrel{电解}{→}$ Mg(s) |
| 键能 | 键能 | 键能 | |||
| H-H | 436 | Cl-Cl | 243 | H-Cl | 432 |
| S=S | 255 | H-S | 339 | C-F | 427 |
| C-Cl | 330 | C-I | 218 | H-F | 565 |
| C-O | 347 | H-O | 464 |
| A. | 键能越大,物质的热稳定性越强 | |
| B. | 热化学方程式H2(g)+Cl2(g)═2HCl(g);△H=-QkJ•mol-1中,Q的值为185 | |
| C. | H-O键的键能大于H-S键的键能,所以H2O的溶沸点高于H2S的溶沸点 | |
| D. | C-Br键的键能应在218kJ•mol-1-330kJ•mol-1之间 |
| A. | 0.05mol Na2O2固体中含有的阴离子数为0.05NA | |
| B. | 标准状况下,2.24L CH4所含的原子数为0.5NA | |
| C. | 1molSO2与足量O2在一定条件下反应,共转移2NA个电子 | |
| D. | 1L0.1mol•L-1氨水中含有的NH3•H2O分子数为0.1NA |
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | ① | |||||||
| 2 | ⑤ | ⑥ | ⑦ | |||||
| 3 | ② | ③ | ④ | ⑧ | ||||
| 4 | ⑨ | |||||||
| 5 | ⑩ |
(2)①和⑦两种元素的原子按1:1组成的常见化合物的结构式为H-O-O-H.
(3)③、④、⑦、⑧的简单离子半径由大到小的顺序为Cl-、O2-、Mg2+、Al3+.(用离子符号表示)
(4)②、④的最高价氧化物的水化物之间发生反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
(5)用电子式表示③和⑨组成的化合物的形成过程
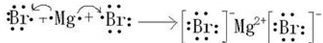 .
.(6)海带中含有⑩元素,海带灰中含有该元素的简单阴离子,在硫酸酸化下,可用双氧水将其氧化为单质.写出该反应的离子方程式2H++H2O2+2I-=2H2O+I2.