题目内容
5.对化学反应的速率和限度的叙述正确的是( )| A. | 增加某一反应物的用量一定能够加快该反应的速率 | |
| B. | 化学反应的限度是不可改变的 | |
| C. | 化学反应达到限度时,正逆反应速率相等 | |
| D. | 化学反应进行的时间越长该反应的限度越大 |
分析 当化学反应达到反应限度时,即达到平衡状态,正逆反应速率相等,各物质的浓度不变,但反应没有停止,当外界条件发生变化时,平衡发生移动,反应限度变化,以此解答该题.
解答 解:A.如增加某一反应中固体物质的用量,不会改变化学反应的速率,故A错误;
B.改变外界条件的温度、压强、浓度可以引起平衡的移动,化学反应的限度是可改变的,故B错误;
C.当化学反应在一定条件下达到限度时,正、逆反应速率相等,但不等于0,故C正确;
D.化学反应进行到一定的时间可以达到平衡状态,时间再长,该反应的转化率不再变化,故D错误.
故选C.
点评 本题考查化学反应速率及影响因素,为高频考点,把握速率的定义、平衡状态的特征及影响因素为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
15.已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,其中aq代表稀溶液,以下四个反应方程式中,反应热△H=-57.3kJ/mol的是( )
| A. | H2SO4(aq)+2NaOH(aq)═Na2SO4(aq)+2H2O(l) | |
| B. | $\frac{1}{2}$H2SO4(aq)+$\frac{1}{2}$Ba(OH)2(aq)═BaSO4(s)+H2O(l) | |
| C. | HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l) | |
| D. | HCl(aq)+NH3•H2O(aq)═NH4Cl(aq)+H2O(l) |
13.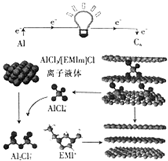 英国《自然》杂志近期报道了一种用泡沫石墨烯(Cn)作正极材料的新型铝离子电池,其放电时的工作原理如图所示.下列说法不正确的是( )
英国《自然》杂志近期报道了一种用泡沫石墨烯(Cn)作正极材料的新型铝离子电池,其放电时的工作原理如图所示.下列说法不正确的是( )
 英国《自然》杂志近期报道了一种用泡沫石墨烯(Cn)作正极材料的新型铝离子电池,其放电时的工作原理如图所示.下列说法不正确的是( )
英国《自然》杂志近期报道了一种用泡沫石墨烯(Cn)作正极材料的新型铝离子电池,其放电时的工作原理如图所示.下列说法不正确的是( )| A. | 放电时,若外电路中转移1mol电子,则负极质量减少9g | |
| B. | 充电时,石墨烯作阳极 | |
| C. | 充电时,阴极的电极反应式为AlCl4-+3e-═Al+4Cl- | |
| D. | 放电时,正极的电极反应式为Cn(AlCl4-)+e-═Cn+AlCl4- |
20.已知下列反应的热化学方程式( )
6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1
2H2(g)+O2(g)═2H2O(g)△H2
C(s)+O2(g)═CO2(g)△H3
则反应4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为( )
6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1
2H2(g)+O2(g)═2H2O(g)△H2
C(s)+O2(g)═CO2(g)△H3
则反应4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为( )
| A. | △H1-5△H2-12△H3 | B. | 2△H1-5△H2-12△H3 | C. | 12△H3-5△H2-2△H1 | D. | 12△H3+5△H2-2△H1 |
10.下列解释事实的方程式不正确的是( )
| A. | 明矾净水:Al3++3H2O?Al(OH)3(胶体)+3H+ | |
| B. | 用稀HNO3清洗试管内壁上的银:Ag+2H++NO3-═Ag++NO2↑+H2O | |
| C. | 实验室盛装NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O | |
| D. | 焊接钢轨:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 |
17.欲配制浓度为1.00mol/L的氯化钠溶液100mL,用不到的仪器是( )
| A. | 100mL容量瓶 | B. | 分液漏斗 | C. | 玻璃棒 | D. | 胶头滴管 |
15.低血糖患者常需补充葡萄糖.组成葡萄糖的元素有( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |

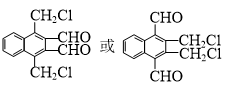 .
.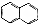 )的衍生物,且取代基都在同一个苯环上;
)的衍生物,且取代基都在同一个苯环上;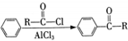 (R为烃基).根据已有知识并结合相关信息,写出以ClCH2CH2CH2Cl和
(R为烃基).根据已有知识并结合相关信息,写出以ClCH2CH2CH2Cl和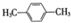 为原料制备
为原料制备 的合成路线流程图(无机试剂可任选).合成路线流程图示例如图所示:
的合成路线流程图(无机试剂可任选).合成路线流程图示例如图所示: