题目内容
下列热化学方程式中的反应热下划线处表示燃烧热的是( )
| A、C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l)△H=-akJ/mol | ||||
B、CH3CH2OH(l)+
| ||||
| C、2CO(g)+O2(g)=CO2(g)△H=-c kJ/mol | ||||
D、NH3(g)+
|
考点:燃烧热
专题:化学反应中的能量变化
分析:在25℃,101 kPa时,1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热.单位为kJ/mol.
1.规定可燃物物质的量为1 mol.(具有可比性)
2.规定必须完全燃烧生成稳定的氧化物.
1.规定可燃物物质的量为1 mol.(具有可比性)
2.规定必须完全燃烧生成稳定的氧化物.
解答:
解:A、C6H12O6(s)完全燃烧生成二氧化碳气体和液态水,同时满足分析中两条件,故A正确;
B、乙醇完全燃烧生成二氧化碳气体和液态水,故B错误;
C、CO的物质的量不是1mol,故C错误;
D、水的状态不是液态,故D错误;
故选A.
B、乙醇完全燃烧生成二氧化碳气体和液态水,故B错误;
C、CO的物质的量不是1mol,故C错误;
D、水的状态不是液态,故D错误;
故选A.
点评:本题考查了燃烧热的热化学方程式,难度不大,注意可燃物的化学计量数为1,必需完全燃烧生成稳定的氧化物即可.

练习册系列答案
相关题目
下列关于平衡常数K的说法中,正确的是( )
| A、在任何条件下,化学平衡常数是一个恒定值 |
| B、从平衡常数K的大小能推断一个反应进行的程度 |
| C、改变反应物浓度或生成物浓度都会改变平衡常数K |
| D、平衡常数K与温度有关,与反应浓度、压强也有关 |
下列物质中,不属于合金的是( )
| A、硬铝(Al、Cu、Mg、Mn、Si ) |
| B、黄铜 |
| C、钢铁 |
| D、水银 |
已知浓H2SO4的密度为1.84g?cm-3,硫酸的质量分数为98%.求浓硫酸中的硫酸的物质的量浓度.下面四个计算式中正确的是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列化学式表示物质分子组成的是( )
| A、Na2O |
| B、CS2 |
| C、Al |
| D、SiC |
下列物质中不能发生水解反应的是( )
| A、乙酸乙酯 | B、淀粉 |
| C、蛋白质 | D、果糖 |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、2.4g金属镁变成镁离子时失去的电子数目为0.1NA |
| B、2g氢气所含分子数目为2NA |
| C、在25C,1.01×1O5Pa时,11.2L氮气所含的原子数目为NA |
| D、含3.01×1023个SO42-的Na2S04容液中,Na+数目为NA |
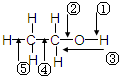 乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明正确的是( )
乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明正确的是( )| A、和金属钠作用时,键②断裂 |
| B、和浓硫酸共热至170℃时,②键和⑤断裂 |
| C、在铜催化下和氧气反应时,键①和③断裂 |
| D、与氢卤酸反应时,键①断裂 |