题目内容
12.对于反应N2+3H2?2NH3(正反应为放热反应),能使正反应速率和逆反应速率增大的因素有:①升高温度、②使用催化剂、③增大压强、④增加N2或和H2的浓度( )| A. | ①②③ | B. | ②③④ | C. | ①②③④ | D. | ①③④ |
分析 根据升温、加压、增大浓度、使用催化剂等可加快化学反应速率,对于可逆反应来说,正逆反应速率的变化趋势是一样的,以此来解答.
解答 解:①升高温度,活化分子的百分数增大,使正、逆化学反应速率加快,故正确;
②使用催化剂,活化分子的百分数增大,使正、逆化学反应速率加快,故正确;
③增大压强,增大活化分子的浓度,反应速率增大,故正确;
④增加N2或H2的浓度,增反应速率增大,但瞬间逆反应速率不变,故错误.
故选A.
点评 本题考查影响化学反应速率的因素,较简单,明确温度、压强、浓度、催化剂等常见的影响因素即可解答.

练习册系列答案
相关题目
3.有Al、CuO、Fe2O3组成的混合物共10.0g,放入200mL某浓度的硫酸溶液中,混合物完全溶解,当再加入280mL 1.0mol•L-1的NaOH溶液时,得到的沉淀最多.上述硫酸溶液的浓度为( )
| A. | 1.4 mol•L-1 | B. | 1.0 mol•L-1 | C. | 0.7 mol•L-1 | D. | 0.5mol•L-1 |
7.下列有关电化学的图示完全正确的是( )
| A. |  海水防止铁被腐蚀 | |
| B. |  CuSO4精铜的精炼 | |
| C. |  ZnCl2溶液铁片镀锌 | |
| D. |  饱和食盐水验证NaCl溶液(含酚酞)电解产物 |
17.1.6克某气体在标准状况下的体积为1.12L,则其相对分子质量为( )
| A. | 16 | B. | 28 | C. | 32 | D. | 48 |
1.下列说法中正确的是( )
| A. | 生成物总能量一定低于反应物总能量 | |
| B. | 同温同压下,H2(g)+Cl2(g)═2HCl(g) 在光照和点燃条件下的△H相同 | |
| C. | 已知N2(g)+3H2(g)═2 NH3(g);△H=-92.4 kJ•mol-1,则在一定条件下将1molN2和3molH2置于一密闭容器中充分反应后,最多可放出92.4kJ的热量 | |
| D. | 在中和热测定试验的操作过程中,应向盛有稀盐酸的小烧杯中逐滴滴加氢氧化钠稀溶液 |
2.下列有关阿伏加德罗常数(NA)的叙述正确的是( )
| A. | 常温常压下,32克氧气中含有2NA个原子 | |
| B. | 标准状况下,1L己烯完全燃烧后所生成气态产物的分子数为6NA/22.4 | |
| C. | 78g Na2O2晶体中含有的阴离子数目为2NA个 | |
| D. | 1molNa2O2与足量CO2反应转移的电子总数为2NA |
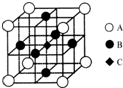 信息一:铬同镍、钴、铁等金属可以构成高温合金、电热合金、精密合金等,用于航空、宇航、电器及仪表等工业部门.
信息一:铬同镍、钴、铁等金属可以构成高温合金、电热合金、精密合金等,用于航空、宇航、电器及仪表等工业部门.