题目内容
1.下列操作不能在氧化铝坩埚中进行的是( )| A. | 加热NH4HCO3 | B. | 加热Fe(OH)3 | C. | 加热NaOH | D. | 加热CaCO3 |
分析 氧化铝是两性氧化物,能溶于强酸和强碱溶液中,所以强碱性固体不能在氧化铝坩埚中熔融,据此分析解答.
解答 解:氧化铝是两性氧化物,能溶于强酸和强碱溶液中,所以强碱性固体不能在氧化铝坩埚中熔融,只有NaOH是强碱,所以NaOH不能在氧化铝坩埚中加热,故选C.
点评 本题考查氧化铝的性质,为高频考点,明确氧化铝两性特点是解本题关键,注意基础知识的总结和归纳,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11. 纯碱、烧碱等是重要的化工原料.
纯碱、烧碱等是重要的化工原料.
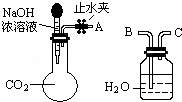
(1)利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应.将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是水沿导管由广口瓶进入烧瓶(或:水倒吸进入烧瓶),反应的离子方程式是2OH-+CO2=CO32-+H2O(或CO2+OH-=HCO3-).若其它操作不变,将A与C连接,可观察到的现象是广口瓶中的长导管口有气泡产生.
(2)向100mL2mol/L的NaOH 溶液中通入一定量CO2,结晶,得到9.3g白色固体,该白色固体的组成是NaOH和Na2CO3(写化学式).
设计实验确认该白色固体中存在的阴离子,试完成下列方案.
(3)在标况下,将4.48L CO2气体通入300mL 1mol/L 的NaOH的稀溶液中,写出该反应的离子方程式(用一个离子方程式表示)2CO2+3OH-=CO32-+HCO3-+H2O.
 纯碱、烧碱等是重要的化工原料.
纯碱、烧碱等是重要的化工原料.(1)利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应.将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是水沿导管由广口瓶进入烧瓶(或:水倒吸进入烧瓶),反应的离子方程式是2OH-+CO2=CO32-+H2O(或CO2+OH-=HCO3-).若其它操作不变,将A与C连接,可观察到的现象是广口瓶中的长导管口有气泡产生.
(2)向100mL2mol/L的NaOH 溶液中通入一定量CO2,结晶,得到9.3g白色固体,该白色固体的组成是NaOH和Na2CO3(写化学式).
设计实验确认该白色固体中存在的阴离子,试完成下列方案.
| 实验操作 | 实验现象 | 结论 |
| ①取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 | 产生白色沉淀 | 有CO32- |
| ②过滤,取2mL滤液于试管中 | ||
| ③滴加酚酞 | 溶液变红 | 有OH- |
12.下列叙述中,不正确的是( )
| A. | 钠原子有强还原性,钠离子有弱氧化性 | |
| B. | 钠离子浓度大的溶液一定显碱性 | |
| C. | 由于钠很活泼,所以一定能从溶液中置换出金属活动性顺序表中钠后面的金属 | |
| D. | 钠是电和热的良导体 |
9.同温同压下,等质量的O2 和O3 相比较,下列结论正确的是( )
| A. | 它们的密度之比为 1:1 | B. | 它们的分子数目之比是 1:1 | ||
| C. | 它们的体积之比是 1:1 | D. | 它们的氧原子数目之比为 1:1 |
16.下列各组混合物中,总质量一定时,二者以不同比例混合,完全燃烧时生成CO2的质量不一定的是( )
| A. | 甲烷、辛醛 | B. | 乙炔、乙烯 | C. | 乙烯、庚烯 | D. | 苯、甲苯 |
6.等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加入等质量的铝,生成氢气的体积比为5:6,则甲、乙两烧杯中的反应情况可能分别是( )
| A. | 甲、乙中都是铝过量 | B. | 甲中铝不足、乙中铝过量 | ||
| C. | 甲中酸过量、乙中铝过量 | D. | 甲中酸过量、乙中铝过量 |
10.下列叙述不正确的是( )
| A. | 纯水也是一种电解质 | |
| B. | 无论是酸性、中性还是碱性稀溶液,只要温度恒定,c(H+)×c(OH-)是一个常数 | |
| C. | 一定温度下,0.1mol•L-1的磷酸溶液中H+主要来自于酸的第一步电离 | |
| D. | 强碱溶液中不存在H+ |