题目内容
3.根据有机化学知识回答问题:Ⅰ.根据图1回答问题:
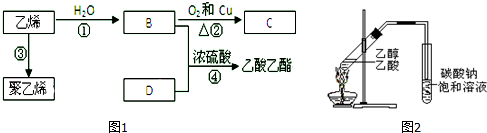
(1)写出乙烯的结构简式CH2═CH2+H2O.
(2)写出B和D中官能团的名称羟基、羧基.
(3)写出反应③的化学反应类型:加聚反应.
(4)写出反应 ①、②的化学反应方程式:CH2═CH2+H2O$→_{△}^{催化剂}$CH3CH2OH,2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+H2O.
Ⅱ.“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图2所示的装置制取乙酸乙酯.回答下列问题:
(1)写出制取乙酸乙酯的化学反应方程式CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O
(2)浓硫酸的作用是:①催化作用;②吸水作用.
(3)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止防止倒吸.
(4)若要把制得的乙酸乙酯分离出来,应采用的实验操作是用饱和碳酸钠溶液承接蒸馏出的乙酸乙酯,再分液.
分析 Ⅰ.乙烯和水反应生成B为CH3CH2OH,CH3CH2OH发生催化氧化生成C为CH3CHO,D与乙醇发生酯化反应生成乙酸乙酯,则D为CH3COOH;
Ⅱ.乙酸、乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯,反应中浓硫酸起到催化剂和吸水剂的作用,饱和碳酸钠溶液用于吸收乙醇、除去乙酸,乙酸乙酯不溶于饱和碳酸钠溶液,可用分液的方法分离,以此解答该题.
解答 解:Ⅰ.乙烯和水反应生成B为CH3CH2OH,CH3CH2OH发生催化氧化生成C为CH3CHO,D与乙醇发生酯化反应生成乙酸乙酯,则D为CH3COOH,
(1)乙烯含有碳碳双键,结构简式为CH2═CH2+H2O,故答案为:CH2═CH2+H2O;
(2)B为乙醇,含有羟基,D为乙酸,含有羧基,故答案为:羟基;羧基;
(3)反应③为乙烯的加聚反应,故答案为:加聚反应;
(4)乙醇和水在催化作用下发生加成反应生成乙醇,方程式为CH2═CH2+H2O$→_{△}^{催化剂}$CH3CH2OH,
乙醇在催化作用下可生成乙醛,方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+H2O,
故答案为:CH2═CH2+H2O$→_{△}^{催化剂}$CH3CH2OH;2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+H2O;
II.(1)乙酸乙醇在浓硫酸催化作用下生成乙酸乙酯,其反应方程式为CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,
故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O;
(2)反应中浓硫酸起到催化和吸水的作用,故答案为:催化作用;吸水作用;
(3)导管不能插入溶液中,导管要插在饱和碳酸钠溶液的液面上,伸入液面下可能发生倒吸,
故答案为:防止倒吸;
(4)乙酸乙酯不溶于饱和碳酸钠溶液,且乙酸与饱和碳酸钠溶液反应而除去,乙醇易溶于水,可用饱和碳酸钠溶液除杂,并用分液的方法分离,
故答案为:用饱和碳酸钠溶液承接蒸馏出的乙酸乙酯,再分液.
点评 本题考查了有机物的推断和有机物的制备实验,注意把握有机物官能团与性质的关系,注意把握实验原理和操作时的注意事项,题目难度中等,侧重于考查学生的实验操作能力和分析问题、解决问题的能力.

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案| A. | X>Y>Z | B. | X>Z>Y | C. | Z>X>Y | D. | Y>Z>X |
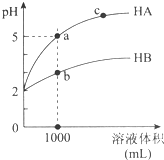 室温下,pH均为2的两种一元酸HA和HB各1mL,分别加水稀释,pH随溶液体积的变化曲线如图所示.下列说法正确的是( )
室温下,pH均为2的两种一元酸HA和HB各1mL,分别加水稀释,pH随溶液体积的变化曲线如图所示.下列说法正确的是( )| A. | HA的酸性比HB的酸性弱 | |
| B. | a点溶液的导电性比c点溶液的导电性弱 | |
| C. | 若两溶液无限稀释,则它们的c(H+)相等 | |
| D. | 对a、b两点溶液同时升高温度,则$\frac{c({A}^{-})}{{c(B}^{-})}$增大 |
| A. | S:3p4 | B. | Cr:3d44s2 | C. | Se:5s25p6 | D. | Cu:3d104s1 |
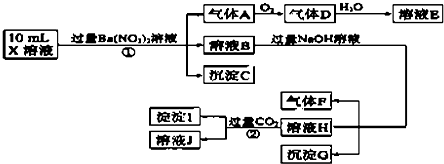
测定A、F、I均为0.1mol,10mL X溶液中n(H+)=0.4mol,沉淀C物质的量小于0.7mol,根据以上信息,下列说法正确的是( )
| A. | 由实验①可知,气体A一定是NO,沉淀C一定是BaSO4,原溶液中肯定含有SO32- | |
| B. | 溶液E和气体F不能发生化学反应 | |
| C. | 由实验 ②可知,沉淀I可能是Al(OH)3和BaCO3 | |
| D. | 原溶液中肯定含有Al3+、NH4+、Fe2+、SO42-、Cl-,不能确定是否含有Fe3+ |
| A. | 铊是银白色的金属 | B. | 能置换出盐酸中氢离子 | ||
| C. | 能生成+3价的化合物 | D. | 氢氧化铊是两性氢氧化物 |
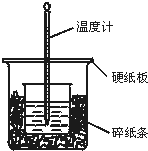 50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: .
.