题目内容
将含O2和CH4的混合气体充入装有23.4gNa2O2的密闭容器中点燃,反应结束后,容器温度为150℃,压强为0pa,将残留物溶于水无气体逸出.下列叙述正确的是( )
分析:反应后压强为0pa,说明容器中无气体,且将残留物溶于水中无气体放出,说明过氧化钠也完全反应,故容器内剩余固体为Na2CO3和NaOH,根据甲烷的组成利用C、H原子守恒可知可知生成的Na2CO3和NaOH物质的量之比为1:4,再根据反应的总化学方程式判断原混合物中甲烷、氧气的物质的量之比.
解答:解:反应后压强为0pa,说明容器中无气体,且将残留物溶于水中无气体放出,说明过氧化钠也完全反应,故容器内剩余固体为Na2CO3和NaOH,
根据甲烷的组成利用C、H原子守恒可知可知生成的Na2CO3和NaOH物质的量之比为1:4,则反应的总化学方程式可写为:2CH4+O2+6Na2O2=2Na2CO3+8NaOH,
根据方程式可知:原混合气体中O2、CH4的物质的量之比为1:2,
故选A.
根据甲烷的组成利用C、H原子守恒可知可知生成的Na2CO3和NaOH物质的量之比为1:4,则反应的总化学方程式可写为:2CH4+O2+6Na2O2=2Na2CO3+8NaOH,
根据方程式可知:原混合气体中O2、CH4的物质的量之比为1:2,
故选A.
点评:本题考查混合物的计算,难度中等,关键是判断剩余固体为Na2CO3和NaOH,利用甲烷的组成确定二者物质的量之比,再利用总方程式解答可以省去中间反应复杂计算的过程.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
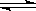 SO3(g);△H=-98 kJ·mol-1。开始时在100 L的密闭容器中加入4.0 mol SO2(g)和10.0 mol O2(g),当反应达到平衡时共放出热量196 kJ,该温度下平衡常数K= 。恒温下,若往容器中再加入4mol SO2(g),则重新达到平衡时SO2的总转化率 原平衡时SO2转化率(选填“>”、“<”或“=”)。
SO3(g);△H=-98 kJ·mol-1。开始时在100 L的密闭容器中加入4.0 mol SO2(g)和10.0 mol O2(g),当反应达到平衡时共放出热量196 kJ,该温度下平衡常数K= 。恒温下,若往容器中再加入4mol SO2(g),则重新达到平衡时SO2的总转化率 原平衡时SO2转化率(选填“>”、“<”或“=”)。