题目内容
煤燃烧的反应热可通过以下两个途径来利用:
Ⅰ.利用煤在充足的空气中直接燃烧产生的反应热;
Ⅱ.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧.这两个过程的热化学方程式为:
Ⅰ.C(s)+O2(g) CO2(g);ΔH=E1 ①
CO2(g);ΔH=E1 ①
Ⅱ.C(s)+H2O(g) CO(g)+H2(g);ΔH=E2 ②
CO(g)+H2(g);ΔH=E2 ②
H2(g)+![]() O2(g)
O2(g) H2O(g);ΔH=E3 ③
H2O(g);ΔH=E3 ③
CO(g)+![]() O2(g)
O2(g) CO2(g);ΔH=E4 ④
CO2(g);ΔH=E4 ④
请填写下列空白:
(1)途径Ⅱ与途径Ⅰ相比有较多的优点,即________;
(2)在上述四个热化学方程式中,________(填编号)反应的ΔH>0;
(3)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量正确的关系是(填序号)________;
A.Ⅰ比Ⅱ多
B.Ⅰ比Ⅱ少
C.Ⅰ与Ⅱ在理论上相同
(4)根据能量守恒定律,E1、E2、E3、E4之间的关系为________.
答案:
解析:
解析:
|
(1)煤的利用率高;变为气体燃料后运输方便;燃烧充分(2分,答对两点即可) (2)②(2分) (3)C(2分) (4)E1=E2+E3+E4(2分) |

练习册系列答案
相关题目
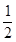 O2(g) = H2O(g) △H=E3 ③
O2(g) = H2O(g) △H=E3 ③