题目内容
19.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )| A. | 7.8 g Na2O2与足量水反应转移的电子数为0.2NA | |
| B. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3NA | |
| C. | 常温常压下,1 mol CH4中含有的氢原子数为4NA | |
| D. | 12.0 g熔融的NaHSO4中含有0.1NA个Na+、0.1NA个H+和0.1NA个SO42- |
分析 A、求出过氧化钠的物质的量,然后根据过氧化钠和水的反应为歧化反应来分析;
B、铁和硝酸反应后最终可能变为+3价,还可能变为+2价;
C、甲烷中含4个H原子;
D、硫酸氢钠在熔融状态下只能电离为钠离子和硫酸氢根离子.
解答 解:A、7.8g过氧化钠的物质的量为0.1mol,而过氧化钠和水的反应为歧化反应,故0.1mol过氧化钠转移0.1mol电子即0.1NA个,故A错误;
B、铁和硝酸反应后最终可能变为+3价,还可能变为+2价,故5.6g铁即0.1mol铁反应后转移的电子数可能为0.3NA个,还可能为0.2NA个,故B错误;
C、甲烷中含4个H原子,故1mol甲烷中含4NA个H原子,故C正确;
D、硫酸氢钠在熔融状态下只能电离为钠离子和硫酸氢根离子,不能电离出氢离子,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.蛋白质的元素组成比油脂多了下列哪种元素( )
| A. | 氢 | B. | 氮 | C. | 氧 | D. | 硅 |
10.下列有关水的说法正确的是( )
| A. | 每一个水分子内含有两个氢键 | |
| B. | 水分子的空间构型为V形 | |
| C. | H2O是一种非常稳定的化合物,这是由于氢键所致 | |
| D. | 水是良好的溶剂,易溶解HCl、CH4等气体 |
7.下列化学现象及解释错误的是( )
| 选项 | 现象 | 解释 |
| A | Cl2在H2中点燃,瓶口有白雾 | 生成HCl极易溶于水 |
| B | 饱和Na2CO3溶液中通入CO2析出白色晶体 | 生成NaHCO3溶解度小析出 |
| C | 常温下将铝片放入浓硝酸中无明显变化 | Al和浓硝酸不反应 |
| D | SO2通入溴水,溴水褪色 | SO2具有还原性. |
| A. | A | B. | B | C. | C | D. | D |
14.已知反应A+B═C+D为放热反应,对该反应的下列说法正确的是( )
| A. | A的能量一定高于C | |
| B. | A和B的总能量一定低于C和D的总能量 | |
| C. | A和B的总能量一定高于C和D的总能量 | |
| D. | 该反应为放热反应,故不必加热就一定能发生 |
4.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向无色溶液中滴加氯水和CCl4,振荡静置 | 下层溶液显紫色 | 溶液中含有I- |
| B | 过量铁粉加入稀硝酸中充分反应,再加入 KSCN溶液 | 溶液呈红色 | 稀硝酸将铁氧化为Fe3+ |
| C | 向BaC12溶液中先通入SO2 | 生成白色沉淀 | 白色沉淀是BaSO4 |
| D | 用玻璃棒蘸取浓硫酸点到蓝色石蕊试纸上 | 试纸先变红后变黑 | 浓硫酸具有酸性和脱水性 |
| A. | A | B. | B | C. | C | D. | D |
9.阿司匹林又名乙酰水杨酸,它的结构式为 ,试推断它不应具有的性质( )
,试推断它不应具有的性质( )
 ,试推断它不应具有的性质( )
,试推断它不应具有的性质( )| A. | 与NaOH溶液反应 | B. | 与金属钠反应 | ||
| C. | 与乙酸发生酯化反应 | D. | 一定条件下发生水解反应 |

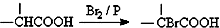
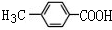 .
.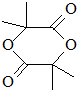 .
.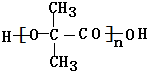 +(n-1)H2O,该反应属于缩聚反应(填反应类型).
+(n-1)H2O,该反应属于缩聚反应(填反应类型). .
. .
.