题目内容
分别用一种试剂将下列物质中混入的少量杂质除去(括号内为混入的杂质)
| 物 质 | 需加入的试剂 | 有关离子方程式 |
| (1)HNO3(H2SO4) | ||
| (2)Cu(Fe) | ||
| (3)NaCl(Na2CO3) |
考点:物质的分离、提纯的基本方法选择与应用,离子方程式的书写
专题:离子反应专题
分析:(1)除去HNO3中的H2SO4,可加入硝酸钡,生成硫酸钡沉淀;
(2)Fe为活泼金属,可与盐酸或稀硫酸反应而除去;
(3)可加入盐酸除去杂质.
(2)Fe为活泼金属,可与盐酸或稀硫酸反应而除去;
(3)可加入盐酸除去杂质.
解答:
解:(1)除去HNO3中的H2SO4,可加入硝酸钡,生成硫酸钡沉淀,反应的离子方程式为Ba2++SO42-=BaSO4↓;
(2)Fe为活泼金属,可与盐酸或稀硫酸反应而除去,反应的离子方程式为Fe+2H+=Fe2++H2↑;
(3)可加入盐酸除去杂质,反应的离子方程式为2H++CO32-=CO2↑+H2O.
故答案为:
(2)Fe为活泼金属,可与盐酸或稀硫酸反应而除去,反应的离子方程式为Fe+2H+=Fe2++H2↑;
(3)可加入盐酸除去杂质,反应的离子方程式为2H++CO32-=CO2↑+H2O.
故答案为:
| Ba(NO3)2 | Ba2++SO42-=BaSO4↓ |
| HCl | Fe+2H+=Fe2++H2↑ |
| HCl | 2H++CO32-=CO2↑+H2O |
点评:本题考查物质的分离提纯,为高频考点,侧重物质除杂及混合物分离方法的考查,把握物质的性质及分离原理为解答的关键,题目难度不大,注意把握离子方程式的书写.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
下列电子式书写错误的是( )
A、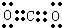 |
B、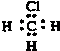 |
C、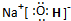 |
D、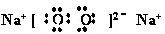 |
设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A、1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
| B、0.1mol丙烯酸中含有双键的数目为0.1NA |
| C、标准状况下,11.2L苯中含有分子的数目为0.5NA |
| D、在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |

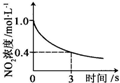
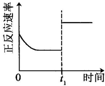
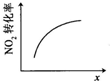

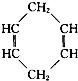 可简写为
可简写为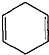 .现有某化合物W的分子结构可表示为
.现有某化合物W的分子结构可表示为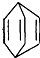 .
.