题目内容
7.已知乙烯能发生以下转化: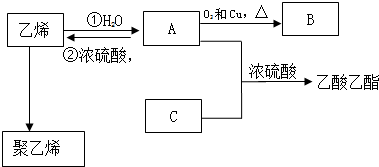
(1)聚乙烯的结构简式为:
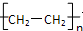 ,化合物C所含官能团的名称为羧基.
,化合物C所含官能团的名称为羧基.(2)写出下列转化的化学方程式(标明反应条件)和反应类型
A→B:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,反应类型:氧化反应.
(3)乙酸乙酯有多种同分异构体,请写出含有酯基的所有同分异构体的结构简式:
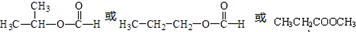 .
.
分析 乙烯和水发生加成反应生成A,A在浓硫酸作催化剂条件下发生消去反应生成乙烯,则A为CH3CH2OH,乙烯发生加聚反应生成聚乙烯,聚乙烯结构简式为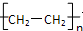 ,A在Cu作催化剂条件下加热发生氧化反应生成B,B为CH3CHO;A和C在浓硫酸作催化剂、加热条件下发生反应生成乙酸乙酯,则C为CH3COOH,据此分析解答.
,A在Cu作催化剂条件下加热发生氧化反应生成B,B为CH3CHO;A和C在浓硫酸作催化剂、加热条件下发生反应生成乙酸乙酯,则C为CH3COOH,据此分析解答.
解答 解:乙烯和水发生加成反应生成A,A在浓硫酸作催化剂条件下发生消去反应生成乙烯,则A为CH3CH2OH,乙烯发生加聚反应生成聚乙烯,聚乙烯结构简式为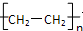 ,A在Cu作催化剂条件下加热发生氧化反应生成B,B为CH3CHO;A和C在浓硫酸作催化剂、加热条件下发生反应生成乙酸乙酯,则C为CH3COOH,
,A在Cu作催化剂条件下加热发生氧化反应生成B,B为CH3CHO;A和C在浓硫酸作催化剂、加热条件下发生反应生成乙酸乙酯,则C为CH3COOH,
(1)聚乙烯的结构简式为: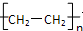 ,C为乙酸,化合物C所含官能团的名称为羧基,
,C为乙酸,化合物C所含官能团的名称为羧基,
故答案为: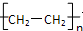 ;羧基;
;羧基;
(2)A在Cu作催化剂条件下加热发生氧化反应生成B,B为CH3CHO,反应方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,反应类型是氧化反应,故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;氧化反应;
(3)乙酸乙酯有多种同分异构体,含有酯基的所有同分异构体的结构简式为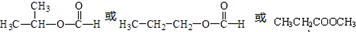 ,
,
故答案为: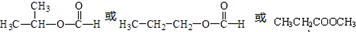 .
.
点评 本题考查有机物推断,为高频考点,明确官能团及其性质关系是解本题关键,注意乙醇的催化氧化反应中水的计量数是2,为易错点.

练习册系列答案
相关题目
17.下列说法不正确的是( )
| A. | 已知冰的熔化热为6.0kJ/mol,冰中氢键键能为20kJ/mol,假设1mol冰中有2mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 | |
| B. | 已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,Ka=$\frac{(ca)^{2}}{c(1-a)}$.若加入少量醋酸钠固体,则CH3COOH?CH3COO-+H+向左移动,α减小,Ka变小 | |
| C. | 实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以证明在苯分子中不存在独立的碳碳双键 | |
| D. | 已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g),△H=+489.0 kJ/mol CO(g)+$\frac{1}{2}$O2(g)═CO2(g),△H=-283.0 kJ/mol. C(石墨)+O2(g)═CO2(g),△H=-393.5 kJ/mol. 则4Fe(s)+3O2(g)═2Fe2O3(s),△H=-1641.0 kJ/mol |
15.已知可逆反应a A(g)+b B(?)?c C(g)△H>0(B物质的状态未确定).关于该反应的描述正确的是( )
| A. | 加压若平衡正向移动,则a>c | |
| B. | 加入一定量的B,平衡一定正向移动 | |
| C. | 缩小容器的体积,各物质的浓度一定增大 | |
| D. | 升高温度,平衡一定正向移动,混合气体的平均摩尔质量的变化不能确定 |
12.下列关于硫及其化合物的说法中正确的是( )
| A. | 自然界中不存在游离态的硫 | |
| B. | SO2和SO3都是酸性氧化物,二者的水溶液都是强酸 | |
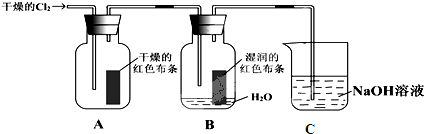
| C. | 浓硫酸可用来干燥SO2、CO、Cl2等气体 | |
| D. | 将铜片放入浓硫酸中,无明显现象是因为铜片发生了钝化 |
19. 请运用化学反应原理的相关知识研究碳及其化合物的性质.
请运用化学反应原理的相关知识研究碳及其化合物的性质.
(1)在一定体积的密闭容器中,进行如下化学反应,CO2(g)+H2(g)?CO(g)+H2O(g),平衡常数K与温度t℃的关系如下表:
①该反应的化学平衡常数表达式为$\frac{c(CO)×c({H}_{2}O)}{c(C{O}_{2})×c({H}_{2})}$.
②该反应为吸热反应(填“吸热”或“放热”).
③某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(2)工业上一般以CO和H2为原料合成甲醇,一定温度下在恒容容器中,该反应的热化学方程式为:
CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1
①下列措施中能说明反应达到平衡状态的是AD.
A.体系压强保持不变
B.混合气体的密度保持不变
C.CO与H2的浓度之比为1:2
D.单位时间内,消耗2molH2的同时消耗1molCH3OH
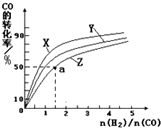
②在恒容容器中合成甲醇,当温度分别为230℃、250℃和270℃时,CO的转化率与n(H2):n(CO)的起始组成比的关系如图所示.已知容器体积1L,起始时CO的物质的量均为1mol.据此判断在上述三种温度中,曲线Z对应的温度是270℃;利用图中a点对应的数据,计算该反应在对应温度下的平衡常数K等于4(mol/L)-2.
 请运用化学反应原理的相关知识研究碳及其化合物的性质.
请运用化学反应原理的相关知识研究碳及其化合物的性质.(1)在一定体积的密闭容器中,进行如下化学反应,CO2(g)+H2(g)?CO(g)+H2O(g),平衡常数K与温度t℃的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
②该反应为吸热反应(填“吸热”或“放热”).
③某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(2)工业上一般以CO和H2为原料合成甲醇,一定温度下在恒容容器中,该反应的热化学方程式为:
CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1
①下列措施中能说明反应达到平衡状态的是AD.
A.体系压强保持不变
B.混合气体的密度保持不变
C.CO与H2的浓度之比为1:2
D.单位时间内,消耗2molH2的同时消耗1molCH3OH
②在恒容容器中合成甲醇,当温度分别为230℃、250℃和270℃时,CO的转化率与n(H2):n(CO)的起始组成比的关系如图所示.已知容器体积1L,起始时CO的物质的量均为1mol.据此判断在上述三种温度中,曲线Z对应的温度是270℃;利用图中a点对应的数据,计算该反应在对应温度下的平衡常数K等于4(mol/L)-2.
 如图,一密闭气缸被一不漏气可滑动的活塞隔成两部分,左室充有氮气,右室充有混合气体.在室温下将右室的气体点燃,反应后冷却至原室温,活塞最终静止于气缸的某一点(液体体积忽略不计).
如图,一密闭气缸被一不漏气可滑动的活塞隔成两部分,左室充有氮气,右室充有混合气体.在室温下将右室的气体点燃,反应后冷却至原室温,活塞最终静止于气缸的某一点(液体体积忽略不计).