题目内容
1.在氢氟酸溶液中,存在下列电离平衡:HF?H++F-,(1)加入NaOH固体后,电离平衡向正(填“正”或“逆”)反应方向移动,C(H+)减小(填“增大”,“减小”或“不变”).
(2)加入NaF固体后,电离平衡向逆(填“正”或“逆”)反应方向移动,C(H+)减小(填“增大”,“减小”或“不变”).
(3)加水稀释,电离平衡向正(填“正”或“逆”)反应方向移动,C(H+)减小(填“增大”,“减小”或“不变”).
分析 在氢氟酸溶液中,存在如下电离平衡:HF?H++F-,升高温度、加水稀释促进弱电解质电离,向弱电解质溶液中加入和氢离子或氟离子反应的物质促进氢氟酸电离,加入含有氢离子或氟离子的物质抑制氢氟酸电离.
解答 解:(1)加入氢氧化钠固体,氢氧化钠和氢离子反应生成水,促进氢氟酸电离,溶液中氢离子浓度减小,
故答案为:正;减小;
(2)向溶液中加入氟化钠固体,氟离子浓度增大,抑制氢氟酸电离,平衡向逆反应方向移动,溶液中氢离子浓度减小,
故答案为:逆;减小;
(3)弱电解质存在电离平衡,加水稀释促进电离,电离平衡正向进行,但平衡状态各微粒的浓度减小,
故答案为:正,减小;
点评 本题考查了弱电解质的电离,明确影响弱电解质电离的因素是解本题关键,难度不大.

练习册系列答案
相关题目
11.下列事实与氢键有关的是( )
| A. | 水结成冰体积膨胀,密度变小 | |
| B. | 水加热到很高的温度都难以分解 | |
| C. | HF、HCl、HBr、HI的热稳定性依次减弱 | |
| D. | CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高 |
16.把A、B、C、D四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池.A、B相连时,A为负极;C、D相连时,D上有气泡逸出;A、C相连时,A极减轻;B、D相连时,B为正极.则四种金属的活动性顺序由大到小排列为( )
| A. | A>B>C>D | B. | A>C>B>D | C. | A>C>D>B | D. | B>D>C>A |
6.下列说法正确的是( )
| A. | 在粗硅的制取中发生反应2C+SiO2$\frac{\underline{\;高温\;}}{\;}$2CO↑+Si,所以非金属性C>Si | |
| B. | 由Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$CO2↑+Na2SiO3可知硅酸的酸性大于碳酸 | |
| C. | 用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO2 | |
| D. | 由H2S+CuSO4═CuS↓+H2SO4可知,氢硫酸的酸性比硫酸强 |
11.已知Cu2+(aq)+MnS(s)?CuS(s)+Mn2+(aq),化工生产中常用MnS(s)作沉淀剂去除废水中的Cu2+.下列有关说法正确的是( )
| A. | 当c(Cu2+)=c(Mn2+)时该反应达到平衡 | |
| B. | 从该反应原理可以得出CuS的溶解度比MnS的溶解度大 | |
| C. | 该反应的平衡常数K=$\frac{{K}_{sp}(MnS)}{{K}_{sp}(CuS)}$ | |
| D. | 往平衡体系中加入少量CuSO4(s)后,c( Mn2+)不变 |
 .
.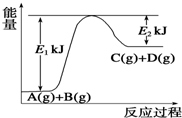 已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题.
已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题.