题目内容
将H2S和O2的混合气体在120℃的温度下装入密闭容器中,在高温下使之燃烧.已知全部H2S和O2都参加了反应,反应后容器内恢复到120℃,测得压强为反应前的
.则原混合气体中H2S与O2的物质的量之比为( )
| 3 |
| 4 |
| A、1:1 | B、1:2 |
| C、1:3 | D、3:2 |
考点:有关混合物反应的计算
专题:
分析:可能发生反应2H2S+O2
2S+2H2O;2H2S+3O2
2SO2+2H2O,据此设原混合气体中H2S、O2分别为x、y,利用质量守恒写出反应xH2S+yO2
(y-
)SO2+(1.5x-y)S+xH2O,气体体积减小了
,再根据差量法计算.
| ||
| ||
| ||
| x |
| 2 |
| 1 |
| 4 |
解答:
解:容器容积不变,恢复到原来温度时,测得压强为反应前的
,则气体体积减少了:1-
=
,
xH2S+yO2
(y-
)SO2+(1.5x-y)S+xH2O 气体体积减少
x y (y-
) x
则
=
,
解得x:y=1:1,
故选A.
| 3 |
| 4 |
| 3 |
| 4 |
| 1 |
| 4 |
xH2S+yO2
| ||
| x |
| 2 |
x y (y-
| x |
| 2 |
| x |
| 2 |
则
| ||
| x+y |
| 1 |
| 4 |
解得x:y=1:1,
故选A.
点评:本题考查了有关反应物过量的计算,题目难度中等,正确书写反应原理为解答本题的关键,明确反应物过量对反应产物的影响,试题培养了学生的分析、理解能力.

练习册系列答案
相关题目
下列化学用语正确的是( )
| A、乙烯的结构简式为:CH2CH2 |
| B、苯酚的分子式为:C6H6O |
| C、羟基的电子式为:-O﹕H |
D、甲烷分子的比例模型: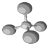 |
下列各物质,按照单质、氧化物、混合物分类,排列正确的是( )
| A、冰、干冰、水玻璃 |
| B、氮气、氧气、小苏打 |
| C、有液氯、冰水、漂粉精 |
| D、氯气、铁红、胆矾 |
700℃时,向容积不变的1L密闭容器中充人一定量的CO和H2O,发生反应:CO(g)+H2O(g)?CO2(g)+H2(g)反应过程中测定的部分数据见下表(表中t1<t2)下列说法不正确的是( )
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
A、O-t1 min的平均反应速率为v(H2)=
| ||
| B、保持其他条件不变,若容器内的压强不改变时,该反应一定达到了化学平衡状态 | ||
| C、保持其他条件不变,若起始时向容器中充入0.60mol CO和1.20mol H2O,则达到平衡时n(CO2)=0.40mol | ||
| D、保持其他条件不变,向平衡体系中再通入0.20mol H2O,与原平衡相比,达到新平衡时CO的转化率增大,CO2的浓度增大 |
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是( )
| A、SO2和SiO2 |
| B、HCl和AlCl3 |
| C、NaCl和NaOH |
| D、CCl4和KCl |
