��Ŀ����
һ���¶��£���һ�����л������ݻ��ɱ���ܱ������У�������һ���������ͨ�����������·�Ӧ��X��g��+3Y��g��
=2Z��g����H��0����Ӧ��ʼʱ����2moIX��8molY���ﵽƽ����ƽ��ʱ�������������ʵ���Ϊ8.4mol��X���������Ϊw%��
��1��д���÷�Ӧƽ�ⳣ���ı���ʽ______��������ƽ��ʱX��ת����______��
��2��������ѹǿ���÷�Ӧ�Ļ�ѧ��Ӧ���ʽ�______���÷�Ӧ��Kֵ��______ �����������С�����䡱����
��3������������Ӧ�¶Ȳ��䣬��a��b��c�ֱ������ʼ�����X��Y��Z�����ʵ���������Ӧ��ƽ����������x�����������Ϊw%����ô��
��a=1��c=2����b=______���ڴ�����·�Ӧ��ʼʱ����______������У�
��4������������Ӧ�¶Ȳ��䣬�����������������Ϊ��ʼ���ʣ���ƽ���X�������������w%����______��������ţ�
A��4molZ B��2.5molX��4.5molY�� 1molZ
C��3molX�� 6molY D��1molX�� 4molZ��
| ||
��1��д���÷�Ӧƽ�ⳣ���ı���ʽ______��������ƽ��ʱX��ת����______��
��2��������ѹǿ���÷�Ӧ�Ļ�ѧ��Ӧ���ʽ�______���÷�Ӧ��Kֵ��______ �����������С�����䡱����
��3������������Ӧ�¶Ȳ��䣬��a��b��c�ֱ������ʼ�����X��Y��Z�����ʵ���������Ӧ��ƽ����������x�����������Ϊw%����ô��
��a=1��c=2����b=______���ڴ�����·�Ӧ��ʼʱ����______������У�
��4������������Ӧ�¶Ȳ��䣬�����������������Ϊ��ʼ���ʣ���ƽ���X�������������w%����______��������ţ�
A��4molZ B��2.5molX��4.5molY�� 1molZ
C��3molX�� 6molY D��1molX�� 4molZ��
��1��ƽ�ⳣ��Ϊ����Ũ��ϵ�����ݵij˻��뷴Ӧ��Ũ��ϵ�����ݵij˻��ı�ֵ������ƽ�ⳣ��K=
��
��ʼX�����ʵ���Ϊ2moIX����
X��g��+3Y��g��
2Z��g�� ���ʵ������١�n
1 2 2
0.8mol 1.6mol 2mol+8mol-8.4mol=1.6mol
���ԣ�ƽ��ʱX��ת����Ϊ
��100%=40%��
�ʴ�Ϊ��K=
��40%
��2������ѹǿ����λ����ڻ����������ѧ��Ӧ��������ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶Ȳ���ƽ�ⳣ�����䣮
�ʴ�Ϊ��������
��3�����������X�����������Ϊw%��Ϊ��Чƽ�⣮���º�ѹ�£���Ӧǰ����������仯������ѧ������ת�����������X��Y�����ʵ���֮��Ϊ1��4��
X��g��+3Y��g��
2Z��g��
1mol 3mol 2mol
���ԣ�1+1������b+3��=1��4�����b=5��
�ɣ�1����֪ƽ��ʱZ���������Ϊ
=
��������µ�Z���������Ϊ
=
��
��
�����Է�Ӧ���淴Ӧ������У�
�ʴ�Ϊ��5���淴Ӧ
��4��ƽ��������Ӧ�ƶ�X�����������С�����淴Ӧ�ƶ�ƽ��ʱX�������������
A����ʼ��4molZ����ЧΪ��ʼ����2moIX��6molY����ԭƽ����ȣ�Y�����ʵ�����С��X��Y�����ʵ���֮��Ϊ1��3������1��4����ԭƽ����ȣ�ƽ�����淴Ӧ�ƶ���X�������������A��ȷ��
B����ʼ����2.5molX��4.5molY�� 1molZ����ЧΪ��ʼ����3moIX��6molY��X��Y�����ʵ���֮��Ϊ1��2������1��4����ԭƽ����ȣ�ƽ�����淴Ӧ�ƶ���X�������������B��ȷ��
C����ʼ����3molX�� 6molY��X��Y�����ʵ���֮��Ϊ1��2������1��4����ԭƽ����ȣ�ƽ�����淴Ӧ�ƶ���X�������������C��ȷ��
D����ʼ����1molX�� 4molZ����ЧΪ��ʼ����3molX��6molY��X��Y�����ʵ���֮��Ϊ1��2������1��4����ԭƽ����ȣ�ƽ�����淴Ӧ�ƶ���X�������������D��ȷ��
��ѡ��ABCD
| c2(Z) |
| c(X)?c3(Y) |
��ʼX�����ʵ���Ϊ2moIX����
X��g��+3Y��g��
| һ������ |
1 2 2
0.8mol 1.6mol 2mol+8mol-8.4mol=1.6mol
���ԣ�ƽ��ʱX��ת����Ϊ
| 0.8mol |
| 2mol |
�ʴ�Ϊ��K=
| c2(Z) |
| c(X)?c3(Y) |
��2������ѹǿ����λ����ڻ����������ѧ��Ӧ��������ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶Ȳ���ƽ�ⳣ�����䣮
�ʴ�Ϊ��������
��3�����������X�����������Ϊw%��Ϊ��Чƽ�⣮���º�ѹ�£���Ӧǰ����������仯������ѧ������ת�����������X��Y�����ʵ���֮��Ϊ1��4��
X��g��+3Y��g��
| ||
1mol 3mol 2mol
���ԣ�1+1������b+3��=1��4�����b=5��
�ɣ�1����֪ƽ��ʱZ���������Ϊ
| 1.6mol |
| 8.4mol |
| 4 |
| 21 |
| 2mol |
| 1mol+5mol+2mol |
| 1 |
| 4 |
| 4 |
| 21 |
| 1 |
| 4 |
�ʴ�Ϊ��5���淴Ӧ
��4��ƽ��������Ӧ�ƶ�X�����������С�����淴Ӧ�ƶ�ƽ��ʱX�������������
A����ʼ��4molZ����ЧΪ��ʼ����2moIX��6molY����ԭƽ����ȣ�Y�����ʵ�����С��X��Y�����ʵ���֮��Ϊ1��3������1��4����ԭƽ����ȣ�ƽ�����淴Ӧ�ƶ���X�������������A��ȷ��
B����ʼ����2.5molX��4.5molY�� 1molZ����ЧΪ��ʼ����3moIX��6molY��X��Y�����ʵ���֮��Ϊ1��2������1��4����ԭƽ����ȣ�ƽ�����淴Ӧ�ƶ���X�������������B��ȷ��
C����ʼ����3molX�� 6molY��X��Y�����ʵ���֮��Ϊ1��2������1��4����ԭƽ����ȣ�ƽ�����淴Ӧ�ƶ���X�������������C��ȷ��
D����ʼ����1molX�� 4molZ����ЧΪ��ʼ����3molX��6molY��X��Y�����ʵ���֮��Ϊ1��2������1��4����ԭƽ����ȣ�ƽ�����淴Ӧ�ƶ���X�������������D��ȷ��
��ѡ��ABCD

��ϰ��ϵ�д�
 ����ѧ����ϵ�д�
����ѧ����ϵ�д�
�����Ŀ
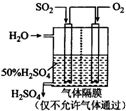 ���ᱻ��Ϊ����ҵ֮ĸ����������ڹ�ҵ�����е���Ҫ��λ�����ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ��������Ĺؼ����裮һ���¶��£���һ�������������Ϊ2L���ܱ������г���2.0mol SO2��g����1.0mol O2��g����������Ӧ��SO2��g��+
���ᱻ��Ϊ����ҵ֮ĸ����������ڹ�ҵ�����е���Ҫ��λ�����ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ��������Ĺؼ����裮һ���¶��£���һ�������������Ϊ2L���ܱ������г���2.0mol SO2��g����1.0mol O2��g����������Ӧ��SO2��g��+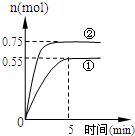 ̼ѭ����;��֮һ�ǣ�CO2��g��+3H2��g��?CH3OH��g��+H2O��g��+49.0kJ�����ݻ�Ϊ2L���ܱ������г���1mol CO2��3mol H2�������ֲ�ͬ��ʵ�������½��з�Ӧ�����CH3OH��g�������ʵ�����ʱ��仯�������ͼ��ʾ��
̼ѭ����;��֮һ�ǣ�CO2��g��+3H2��g��?CH3OH��g��+H2O��g��+49.0kJ�����ݻ�Ϊ2L���ܱ������г���1mol CO2��3mol H2�������ֲ�ͬ��ʵ�������½��з�Ӧ�����CH3OH��g�������ʵ�����ʱ��仯�������ͼ��ʾ��
