题目内容
埋在地下的输油铸铁管道,在下列各种情况下被腐蚀速率最慢的是
| A.在潮湿疏松的土壤中 | B.在含铁元素较多的酸性土壤中 |
| C.在干燥致密不透气的土壤中 | D.在含碳较多的潮湿透气的中性土壤中 |
C
解析试题分析:A、潮湿疏松的土壤中,易和氧气和水接触,腐蚀较快,错误;B、酸性条件下腐蚀较快,错误;C、干燥致密不透气的土壤,水及氧气较少,腐蚀最慢,正确;D、在含碳较多的潮湿透气的中性土壤中,形成原电池,铁腐蚀最快,错误。
考点:铁腐蚀的条件。

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
全钒液流电池是一种新型的绿色环保储能电池,该电池性能优良,其电池总反应为:V3++VO2++H2O VO2++2H++V2+。下列叙述正确的是 ( )
VO2++2H++V2+。下列叙述正确的是 ( )
| A.充电时阳极附近溶液的酸性减弱 |
| B.充电时阳极反应式为:VO2++2H++e-=VO2++H2O |
| C.放电过程中电解质溶液中阳离子移向负极 |
| D.放电时每转移1mol电子,负极有1mol V2+被氧化 |
电解法精炼含有Fe、Zn、Ag等杂质的粗铜。下列叙述正确的是
| A.电解时以硫酸铜溶液作电解液,精铜作阳极 |
| B.粗铜与电源负极相连,发生氧化反应 |
| C.阴极上发生的反应是Cu2++2e-=Cu |
| D.电解后Fe、Zn、Ag等杂质会沉积在电解槽底部形成阳极泥 |
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为: Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是( )
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为:2MnO2+H2O+2e—→Mn2O3+2OH— |
| C.外电路中每通过O.2mol电子,锌的质量理论上减小6.5g[ |
| D.电池工作时,电子由负极通过电解液流向正极 |
电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极极板,通过导线与直流电源相连。下列说法不正确的是 ( )
| A.若电镀铜,则Y为铜电极,电解液a可以是硫酸铜或氯化铜溶液 |
| B.若X为铁电极、Y为石墨电极,电解饱和氯化钠溶液一段时间,在两极分别滴加酚酞,X极变红色 |
| C.若用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.1mol的氢氧化铜溶解,刚好恢复到通电前的浓度,则电解过程中转移的电子为0.2mol |
| D.若X、Y为铂电极,a溶液为250mL CuSO4和KNO3的混合液,经过一段时间后,两极均得到标准状况下5.6L气体,则原混合液中CuSO4的物质的量浓度为1mol·L-1 |
298K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+ 立即被还原 成Fe2+。据此某学习小组设计如图所示的原电池装置。下列有关说法正确的是:
| A.正极反应为Zn-2e-→Zn2+ |
| B.左烧杯中溶液的红色变浅 |
| C.Pt电极上有气泡出现 |
| D.该电池总反应为3Zn+2Fe3+=2Fe+3Zn2+ |
下面各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )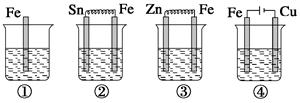
| A.②>①>③>④ | B.④>②>①>③ |
| C.④>②>③>① | D.③>②>④>① |
用惰性电极电解物质的量浓度相等的CuSO4、NaCl混合溶液,电解过程中不可能发生的反应是
A.2Cl-+Cu2+ Cu+Cl2↑ Cu+Cl2↑ |
B.2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
C.2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
D.2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
 Fe(OH)2+Ni(OH)2,下列对该蓄电池推断错误的是:
Fe(OH)2+Ni(OH)2,下列对该蓄电池推断错误的是: