题目内容
NA表示阿伏加德罗常数,下列说法中正确的是( )
| A、0.1mol烷烃(CnH2n+2)中含有共用电子对为0.3nNA |
| B、0.6gCaCO3与KHCO3的混合物中所含质子数为0.3NA |
| C、标准状况下,2.24L乙醛完全燃烧所得CO2分子数为0.2NA |
| D、电解精炼铜时,电解池中每转移1mol电子时,阳极上溶解的铜原子数为0.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.CnH2n+2分子中含有(2n+2)个 C-H 键,(n-1)个 C-C 键,共有 3n+1个共用电子对;
B.1 molCaCO3和KHCO3均含有50 mol的质子;
C.乙醛在标准状况下是液体;
D.比铜活泼的锌、铁等金属先溶解.
B.1 molCaCO3和KHCO3均含有50 mol的质子;
C.乙醛在标准状况下是液体;
D.比铜活泼的锌、铁等金属先溶解.
解答:
解:A.0.1mol烷烃(CnH2n+2)中含有共用电子对为0.1(3n+1)NA,故A错误;
B.两种物质的摩尔质量均为100 g/mo1,混合物共为0.006 mol,而1 molCaCO3和KHCO3均含有50 mol的质子,故B正确;
C.乙醛在标准状况下是液体,2.24L乙醛的物质的量不是1mol,故C错误;
D.阳极上溶解的不仅仅是铜,还有比铜活泼的锌、铁等金属,因此实际溶解的铜少于0.5NA,故D错误.
故选B.
B.两种物质的摩尔质量均为100 g/mo1,混合物共为0.006 mol,而1 molCaCO3和KHCO3均含有50 mol的质子,故B正确;
C.乙醛在标准状况下是液体,2.24L乙醛的物质的量不是1mol,故C错误;
D.阳极上溶解的不仅仅是铜,还有比铜活泼的锌、铁等金属,因此实际溶解的铜少于0.5NA,故D错误.
故选B.
点评:本题考查阿伏加德罗常数,题目难度中等,注意根据物质的结构、组成、聚集状态解题.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
需要加入氧化剂才能发生的变化是( )
| A、HCO3-→CO2 |
| B、Cl-→Cl2 |
| C、MnO4-→Mn2+ |
| D、Fe3+→Fe2+ |
 用右图表示的一些物质或概念之间的从属或包含关系中不正确的是( )
用右图表示的一些物质或概念之间的从属或包含关系中不正确的是( )| X | Y | Z | |
| 例 | 氧化物 | 化合物 | 纯净物 |
| A | 苯 | 芳香烃 | 有机化合物 |
| B | 溶液 | 分散系 | 混合物 |
| C | 强电解质 | 电解质 | 化合物 |
| D | 置换反应 | 氧化还原反应 | 离子反应 |
| A、A | B、B | C、C | D、D |
常温时,下列各组离子在指定溶液中一定能够大量共存的是( )
| A、pH=0的溶液中:Ca2+、Al3+、ClO-、Cl- |
| B、含有大量AlO2-的溶液中:K+、Ca2+、Br-、HCO3- |
| C、加入Mg能放出H2的溶液中:Na+、NH4+、Cl-、SO42- |
| D、酚酞显无色的溶液中:K+、Fe3+、NO3-、SO42- |
下列做法存在安全隐患的是( )
①将水沿烧杯内壁缓缓加入浓硫酸中,用玻璃棒不断搅拌.
②实验室制取氯气时,尾气用碱液吸收.
③取用金属钠或钾做完实验后,剩余的药品要放回原瓶.
④夜间厨房发生煤气泄漏时,立即开灯检查煤气泄漏原因,然后打开所有的门窗通风.
⑤干冰可用于钠、钾、镁等金属的灭火.
①将水沿烧杯内壁缓缓加入浓硫酸中,用玻璃棒不断搅拌.
②实验室制取氯气时,尾气用碱液吸收.
③取用金属钠或钾做完实验后,剩余的药品要放回原瓶.
④夜间厨房发生煤气泄漏时,立即开灯检查煤气泄漏原因,然后打开所有的门窗通风.
⑤干冰可用于钠、钾、镁等金属的灭火.
| A、①④⑤ | B、①②③④ |
| C、①③④⑤ | D、全部 |
下列离子方程式书写正确的是( )
| A、氯气跟水反应:Cl2+H2O→2H++Cl-+ClO- |
| B、硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-→BaSO4↓ |
| C、次氯酸钠溶液中通入CO2:ClO-+CO2+H2O→HCO3-+HClO |
| D、碳酸钙中加入醋酸:CO32-+2CH3COOH→CO2↑+2CH3COO-+H2O |

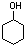 )是一种有机化工基础原料,工业上的主要合成途径及有关反应如下:
)是一种有机化工基础原料,工业上的主要合成途径及有关反应如下: