题目内容
15.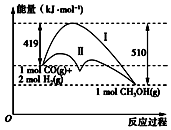 利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)=CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )
利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)=CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )| A. | 该反应物△H=+91 kJ•mol-1 | |
| B. | 加入催化剂,该反应的△H变小 | |
| C. | 曲线Ⅱ使用催化剂,降低了反应的活化能 | |
| D. | 如果该反应生成液态CH3OH,则△H增大 |
分析 A.焓变等于正逆反应活化能之差;
B.催化剂对平衡移动无影响,不改变始终态;
C.催化剂降低反应所需的活化能;
D.液态CH3OH比气态CH3OH的能量低,则反应放出更多,焓变为负.
解答 解:A.焓变等于正逆反应活化能之差,由图可知为放热反应,则△H=(419kJ/mol)-(510kJ/mol)=-91 kJ•mol-1,故A错误;
B.催化剂对平衡移动无影响,不改变始终态,则加入催化剂,该反应的△H不变,故B错误;
C.催化剂降低反应所需的活化能,则曲线Ⅱ使用催化剂,故C正确;
D.液态CH3OH比气态CH3OH的能量低,则反应放出更多,焓变为负,则该反应生成液态CH3OH,则△H减小,故D错误;
故选C.
点评 本题考查反应热与焓变,为高频考点,把握图中能量变化、焓变的计算为解答的关键,侧重分析与应用能力的考查,注意状态与能量的关系,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列分子中只存在σ键的是( )
| A. | CS2 | B. | SiH4 | C. | C2H2 | D. | O2 |
6.下列过程属于物理变化的是( )
| A. | 碳在氧气中燃烧 | B. | 石油的分馏 | C. | 煤的干馏 | D. | 金属钠溶于水 |
3.化学与能源开发、环境保护、资源利用等密切相关.下列说法正确的是( )
| A. | 天然气、石油、流水、风力、氢气为一次能源 | |
| B. | 无论是风力发电还是火力发电,都是将化学能转化为电能 | |
| C. | PM2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素 | |
| D. | 垃圾是放错地方的资源,应分类回收利用 |
20.下列有关原子结构和元素周期律的表述正确的是( )
①短周期元素中正负化合价代数和为4的元素原子为S
②ⅦA族元素是同周期中非金属性最强的元素
③同周期元素原子半径从左到右依次增大
④同主族元素原子从上到下金属性依次减弱,非金属性依次增强.
①短周期元素中正负化合价代数和为4的元素原子为S
②ⅦA族元素是同周期中非金属性最强的元素
③同周期元素原子半径从左到右依次增大
④同主族元素原子从上到下金属性依次减弱,非金属性依次增强.
| A. | ①② | B. | ①③ | C. | ②④ | D. | ③④ |
7.为证明铁的金属活动性比铜强,某同学设计了如下一些方案:
能根据以上各种现象或产物证明铁的金属活动性比铜强的方案共有( )
| 方案 | 现象或产物 |
| ①将铁片置于CuSO4溶液中 | 铁片上有亮红色物质析出 |
| ②将铁丝和铜丝分别在氯气中点燃 | 产物分别为FeC13和CuC12 |
| ③将铁片和铜片分别放入热浓硫酸中 | 产物分别为Fe2(SO4)3和CuSO4 |
| ④将铜片置于FeC13溶液中 | 铜片逐渐溶解 |
| ⑤将铁片和铜片插入盛有稀硫酸的烧杯中,并用导线连接 | 铁片溶解,铜片上有气泡产生 |
| A. | 2 种 | B. | 3 种 | C. | 4种 | D. | 5 种 |
4.常温下,Ka (HCOOH)=1.77×10-4,Ka (CH3COOH)=1.75×10-5,下列说法正确的是( )
| A. | 用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积相等 | |
| B. | 浓度均为0.1 mol•L-1的 HCOONa和NaCl溶液中阴离子的物质的量浓度之和:前者大于后者 | |
| C. | 0.2 mol•L-1 CH3COONa 与 0.1 mol•L-1盐酸等体积混合后的溶液 (pH<7)中,某些粒子浓度大小关系:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| D. | 0.4 mol•L-1 HCOOH 与 0.2 mol•L-1 NaOH 等体积混合后的溶液中,某些粒子浓度大小关系:c(HCOO-)+c(OH-)=c(HCOOH)+c(H+) |
4.关于化学键的下列叙述中,正确的是( )
| A. | 离子化合物可能含共价健 | |
| B. | 离子化合物中一定不含共价键,阳离子只能是金属离子 | |
| C. | 共价化合物可能含离子键 | |
| D. | 有化学键断裂就一定有化学键形成 |