题目内容
2.如图是某燃煤发电厂处理废气的装置示意图,下列说法错误的是( )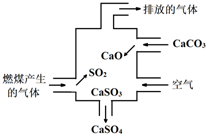
| A. | 使用此装置可减少导致酸雨的气体形成 | |
| B. | 用酸性高锰酸钾溶液检验废气处理是否达标 | |
| C. | 整个过程的总反应可表示为:2SO2+2CaCO3+O2=2CaSO4+2CO2 | |
| D. | 排放的气体是纯净物 |
分析 A、二氧化硫是形成酸雨的重要物质;
B、酸性高锰酸钾溶液褪色说明气体不达标;
C、根据反应过程可以书写反应的化学方程式;
D、根据图示中的信息判断.
解答 解:A、二氧化硫是形成酸雨的重要物质,经过处理后能减少酸雨的形成.故A正确;
B、二氧化硫能使酸性高锰酸钾溶液褪色,所以可用酸性高锰酸钾溶液检验废气处理是否达标,故B正确;
C、整个过程中,二氧化硫与碳酸钙和氧气反应生成了硫酸钙和二氧化碳,化学反应式可表示为:2SO2+2CaCO3+O2=2CaSO4+2CO2,故C正确;
D、根据图示信息可知,进入烟囱的是洁净的气体,洁净并不代表是纯净物,故D错误;
故选D.
点评 本题考查废气的处理,解答本题要充分理解处理废气的过程,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
12.能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是( )
| A. | 向水中投入一小块金属钠 | B. | 将水加热煮沸 | ||
| C. | 向水中通入HCl气体 | D. | 向水中加食盐晶体 |
13.在一个容积固定为2L的密闭容器中,发生反应:aA(g)+bB(g)?pC(g)△H=?,反应情况记录如表:
请根据表中数据仔细分析,回答下列问题:
(1)第2min到第4min内A的平均反应速率v(A)=0.1mol•L-1•min-1
(2)由表中数据可知反应在第4min到第6min时处于平衡状态,若在第2min、6min时分别改变了某一个反应条件,则改变的条件分别可能是:①第 2min使用催化剂、升高温度;②第 6min增加B的浓度;
(3)反应在第4min建立平衡,此温度下该反应的化学平衡常数 K=2.22.
(4)判断第9min时否(是/否)达平衡,说明理由因为Qc<K.
| 时间(min) | n(A)(mol) | n(B)(mol) | n(C)(mol) |
| 0 | 1 | 3 | 0 |
| 第2min | 0.8 | 2.6 | 0.4 |
| 第4min | 0.4 | 1.8 | 1.2 |
| 第6min | 0.4 | 1.8 | 1.2 |
| 第8min | 0.1 | 2.0 | 1.8 |
| 第9min | 0.05 | 1.9 | 0.3 |
(1)第2min到第4min内A的平均反应速率v(A)=0.1mol•L-1•min-1
(2)由表中数据可知反应在第4min到第6min时处于平衡状态,若在第2min、6min时分别改变了某一个反应条件,则改变的条件分别可能是:①第 2min使用催化剂、升高温度;②第 6min增加B的浓度;
(3)反应在第4min建立平衡,此温度下该反应的化学平衡常数 K=2.22.
(4)判断第9min时否(是/否)达平衡,说明理由因为Qc<K.
17.分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是( )
| A. | H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物 | |
| B. | HClO、H2SO4(浓)、HNO3均具有氧化性,都是氧化性酸 | |
| C. | HF、HClO、NH3都易溶于水,都是电解质 | |
| D. | C2H2、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸 |
7.下列离子方程式书写正确的是( )
| A. | 漂白粉溶液中通入过量的CO2:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO | |
| B. | 氯气与水的反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| D. | 钠和冷水反应:Na+2H2O═Na++2OH?+H2↑ |
14.只用一种试剂就能将甲苯、己烯、四氯化碳、碘化钾溶液区分开,该试剂可以是( )
| A. | 酸性高锰酸钾溶液 | B. | 溴化钾溶液 | ||
| C. | 溴水 | D. | 硝酸银溶液 |
11.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:
请回答下列问题:
(1)该反应的化学平衡常数表达式K=$\frac{c(CO)•c(H{\;}_{2}O)}{c(CO{\;}_{2})•c(H{\;}_{2})}$.
(2)该反应为吸热反应(填“吸热”或“放热”),升高温度,逆反应速率增大(填“增大”、“减小”或“不变”)
(3)温度不变,减小CO浓度,平衡向正反应方向移动(填“正反应”或“逆反应”),该反应平衡常数K 值不变(填“增大”、“减小”或“不变”)
(4)800℃时,固定容积的密闭容器中放入混合物,起始浓度为c(CO)=1mol•L-1,c(H2O)=3mol•L-1,c(CO2)=1mol•L-1,c(H2)=5mol•L-1,则反应开始时,H2O的消耗速率比生成速率小(填“大”、“小”或“不能确定”)
(5)t℃时,在2L的固定容积的密闭容器中放入4mol CO2和6mol H2,平衡后CO2的转化率为60%,则达到平衡时CO的体积分数为24%,反应温度t为830℃.
温度不变,若起始时投入3.6mol CO、3.6mol H2O和1.8mol H2,则达到平衡时CO的体积分数为24%,H2的平衡浓度为1.62mol/L.
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式K=$\frac{c(CO)•c(H{\;}_{2}O)}{c(CO{\;}_{2})•c(H{\;}_{2})}$.
(2)该反应为吸热反应(填“吸热”或“放热”),升高温度,逆反应速率增大(填“增大”、“减小”或“不变”)
(3)温度不变,减小CO浓度,平衡向正反应方向移动(填“正反应”或“逆反应”),该反应平衡常数K 值不变(填“增大”、“减小”或“不变”)
(4)800℃时,固定容积的密闭容器中放入混合物,起始浓度为c(CO)=1mol•L-1,c(H2O)=3mol•L-1,c(CO2)=1mol•L-1,c(H2)=5mol•L-1,则反应开始时,H2O的消耗速率比生成速率小(填“大”、“小”或“不能确定”)
(5)t℃时,在2L的固定容积的密闭容器中放入4mol CO2和6mol H2,平衡后CO2的转化率为60%,则达到平衡时CO的体积分数为24%,反应温度t为830℃.
温度不变,若起始时投入3.6mol CO、3.6mol H2O和1.8mol H2,则达到平衡时CO的体积分数为24%,H2的平衡浓度为1.62mol/L.
8.下列物质间的转化不可能通过一步反应实现的是( )
| A. | 铜→氧化铜 | B. | 氢氧化钙→氢氧化钠 | ||
| C. | 铜→碳酸铜 | D. | 碳酸钙→氯化钙 |
