题目内容
某溶液中含有Fe2+和Fe3+,其浓度都是0.050 mol?L-1。如果要求Fe3+沉淀完全而Fe2+不生成Fe(OH)2,需控制pH为何值?已知当溶液中Fe3+浓度降到1.0×10-5mol?L-1时,可以认为Fe3+已沉淀完全;Ksp[Fe(OH)3]=1.1×10-36mol4?L-4,Ksp[Fe(OH)2]=1.64×10-14mol3?L-3。见试题分析
【试题分析】
Fe3+沉淀完全时[Fe3+]不超过1.0×10-5mol?L-1,则Fe3+沉淀完全时所需[OH]-的最小值为:
[OH-]=
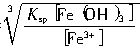 =
= mol?L-1
mol?L-1=4.8×10-11mol?L-1
pH=14-pOH=14-[-lg(4.8×10-11)]=3.7,此即为所控制溶液pH的下限。
Fe2+开始沉淀时所需[OH-]为:
[OH-]=
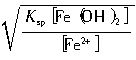 =
=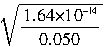 mol?L-1
mol?L-1=5.7×10-7mol?L-1
pH=14-pOH=14-[-lg(5.7×10-7)]=7.8,此即为所控制溶液pH的上限。
故需使Fe3+沉淀完全,Fe2+不沉淀,溶液pH的控制范围为3.7~7.8。

练习册系列答案
相关题目
为了验证某溶液中含有Fe2+而不含有Fe3+,正确的方法是( )
| A、直接滴加KSCN溶液 | B、先滴入KSCN溶液,再通入氯气 | C、先通入足量氯气再滴入KSCN溶液 | D、先加入足量铁粉,充分振荡后再滴加KSCN溶液 |