题目内容
9.下列组合构成原电池装置,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的哪一组( )| A. | A是锌,B是铜,C为稀H2SO4 | B. | A是铜,B是锌,C为稀H2SO4 | ||
| C. | A是铁,B是银,C为AgNO3溶液 | D. | A是Ag,B是铁,C为AgNO3溶液 |
分析 原电池中负极的活泼性大于正极的活泼性,负极上金属失电子变成离子进入溶液,质量减少,正极上得电子发生还原反应,正极上析出物质,若析出的物质是金属,则正极质量增加,据此分析.
解答 解:该原电池中,A极逐渐变粗,B极逐渐变细,所以B作负极,A作正极,B的活泼性大于A的活泼性,所以排除AC选项;
A极逐渐变粗,说明有金属析出,B选项析出氢气不是金属,D选项析出金属,所以D符合题意.
故选D.
点评 本题考查了原电池原理,难度不大,明确正负极的判断方法,注意不能仅根据金属的活泼性判断正负极,要根据发生反应的反应类型判断正负极.

练习册系列答案
相关题目
19.下列元素属于第ⅦA族的是( )
| A. | 钠 | B. | 氯 | C. | 硫 | D. | 硅 |
20.只用一种试剂,区别甲苯、己烯、四氯化碳、乙醇溶液,可选用的试剂是( )
| A. | 硝酸银溶液 | B. | 溴水 | C. | 澄清石灰水 | D. | 酸性高锰酸钾 |
17.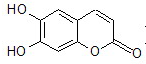 中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和H2溶液完全反应,则消耗的Br2和H2的物质的量分别为( )
中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和H2溶液完全反应,则消耗的Br2和H2的物质的量分别为( )
 中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和H2溶液完全反应,则消耗的Br2和H2的物质的量分别为( )
中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和H2溶液完全反应,则消耗的Br2和H2的物质的量分别为( )| A. | 2mol Br2、3mol H2 | B. | 2mol Br2、4mol H2 | ||
| C. | 3mol Br2、4mol H2 | D. | 4mol Br2、5mol H2 |
4.关于如图所示装置的叙述,正确的是( )
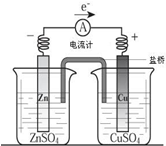

| A. | 铜离子在铜片表面被还原 | B. | 铜是阳极,铜片上有气泡产生 | ||
| C. | 铜片质量逐渐减少 | D. | 电流从锌片经导线流向铜片 |
18. 用如图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )
用如图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )
 用如图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )
用如图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )| 气体 | a | b | c | |
| A | NO2 | 浓硝酸 | 铜片 | NaOH溶液 |
| B | SO2 | 浓硫酸 | 铜片 | 酸性高锰酸钾溶液 |
| C | NH3 | 浓氨水 | 生石灰 | 碱石灰 |
| D | CO2 | 稀盐酸 | 大理石 | 浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
19.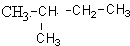 的命名正确的是( )
的命名正确的是( )
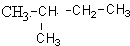 的命名正确的是( )
的命名正确的是( )| A. | 3-甲基丁烷 | B. | 2-甲基戊烷 | C. | 2-甲基丁烷 | D. | 1,1-二甲基丙烷 |
 .
. +HCO3-→
+HCO3-→ +H2O+CO2↑.
+H2O+CO2↑.