题目内容
4.关于如图所示装置的叙述,正确的是( )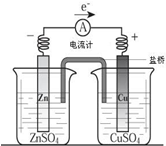
| A. | 铜离子在铜片表面被还原 | B. | 铜是阳极,铜片上有气泡产生 | ||
| C. | 铜片质量逐渐减少 | D. | 电流从锌片经导线流向铜片 |
分析 没有外加电源,所以该装置是原电池.原电池中,活泼性较强的锌作负极,锌失去电子变成离子进入溶液,所以锌片质量减少;活泼性较差的铜作正极,铜离子得电子生成铜单质,附着在铜片上,所以铜片质量增加;电子从锌片沿导线流向铜片,电流从铜片沿导线流向锌片,据此分析.
解答 解:没有外加电源,所以该装置是原电池.原电池中,活泼性较强的锌作负极,锌失去电子变成离子进入溶液,所以锌片质量减少;活泼性较差的铜作正极,铜离子得电子生成铜单质,附着在铜片上,所以铜片质量增加;电子从锌片沿导线流向铜片,电流从铜片沿导线流向锌片.
A、铜是正极,铜离子得电子发生还原反应生成铜单质,所以铜离子在铜片表面被还原,故A正确;
B、铜是正极,铜离子得电子发生还原反应生成铜单质,故B错误.
C、活泼性较差的铜作正极,铜离子得电子生成铜单质,附着在铜片上,所以铜片质量增加,故C错误.
D、电流从铜片沿导线流向锌片,故D错误.
故选A.
点评 本题考查原电池的工作原理,题目难度不大,本题注意把握原电池正负极的判断以及电子、电流的流向.

练习册系列答案
相关题目
14.二十世纪化学合成技术的发展对人类健康水平和生活质量的提高做出了巨大贡献.下列各组物质全部由化学合成得到的是( )
| A. | 玻璃 纤维素 青霉素 | B. | 石英 橡胶 磷化铟尿素 | ||
| C. | 食盐 聚乙烯 | D. | 涤纶 洗衣粉 阿司匹林 |
15.生活中常常碰到涉及化学知识的某些问题,下列叙述错误的是( )
| A. | 人的皮肤在强紫外线的照射下将会失去生理活性 | |
| B. | 常用新制的氢氧化铜检验司机酒后驾车 | |
| C. | 棉花和木材的主要成分都是纤维素 | |
| D. | 蜂蚁叮咬人的皮肤时将分泌物甲酸注入人体,此时可在患处涂抹小苏打或稀氨水 |
12.下列说法不正确的是( )
| A. | 葡萄糖能够发生银镜反应 | |
| B. | 米酒变酸的过程涉及了氧化反应 | |
| C. | 漂白液的有效成分是NaClO,可用于杀菌消毒 | |
| D. | 光导纤维、棉花、油脂、树脂都是由高分子化合物组成的物质 |
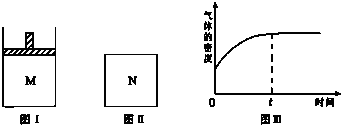
19.在恒压密闭容器M(如图Ⅰ)和恒容密闭容器N(如图Ⅱ)中,分别加入a molA和a molB,起始时两容器体积均为V L,发生如下反应并达到化学平衡状态:
2A(?)+B(?)?xC(g)△H<0
平衡时M中A、B、C的物质的量之比为1:3:2.下列判断正确的是( )
2A(?)+B(?)?xC(g)△H<0
平衡时M中A、B、C的物质的量之比为1:3:2.下列判断正确的是( )

| A. | x=4 | |
| B. | 若N中气体的密度如图Ⅲ所示,则A、B都是气态 | |
| C. | 若A为气体,B为非气体,则平衡时M、N中C的物质的量相等 | |
| D. | 若A、B均为气体,平衡时M中A的转化率大于N中A的转化率 |
9.下列组合构成原电池装置,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的哪一组( )
| A. | A是锌,B是铜,C为稀H2SO4 | B. | A是铜,B是锌,C为稀H2SO4 | ||
| C. | A是铁,B是银,C为AgNO3溶液 | D. | A是Ag,B是铁,C为AgNO3溶液 |
13.下列反应必须用稀硫酸,而不能用浓硫酸的是( )
| A. | 用纤维素制硝化纤维 | B. | 跟苯、浓硝酸作用制硝基苯 | ||
| C. | 溶解金属铜 | D. | 锌与酸制氢气 |
14.下列说法错误的是( )
| A. | 氨是极性分子,其在水中的溶解度很大 | |
| B. | DNA中的碱基互补配对是通过氢键来实现的 | |
| C. | 气体单质中,一定有σ键,可能有π键 | |
| D. | 元素“氦、铷、铯”等是用光谱分析方法发现的 |
 (1)炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑.请回答:铁锅的锈蚀是吸氧腐蚀(填“析氢”或“吸氧”).写出铁锅腐蚀正极的电极反应式:2H2O+O2+4e-=4OH-
(1)炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑.请回答:铁锅的锈蚀是吸氧腐蚀(填“析氢”或“吸氧”).写出铁锅腐蚀正极的电极反应式:2H2O+O2+4e-=4OH-