题目内容
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、22.4L O2中含有氧分子的个数为2NA |
| B、56g Fe与足量氯气反应转移的电子数为2NA |
| C、4g氦气中含有氦原子的个数为NA |
| D、1mol?L-1 MgCl2溶液中含有氯离子个数为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.没有告诉在标准状况下,不能使用标况下的气体摩尔体积计算22.4L氧气的物质的量;
B.铁与氯气反应生成氯化铁,1mol铁完全反应生成3mol电子;
C.稀有气体为单原子分子,4g氦气的物质的量为1mol,1mol氦气含有1mol氦原子;
D.没有告诉氯化镁溶液的体积,无法计算溶液中氯离子数目.
B.铁与氯气反应生成氯化铁,1mol铁完全反应生成3mol电子;
C.稀有气体为单原子分子,4g氦气的物质的量为1mol,1mol氦气含有1mol氦原子;
D.没有告诉氯化镁溶液的体积,无法计算溶液中氯离子数目.
解答:
解:A.不是标准状况下,不能使用标况下的气体摩尔体积计算22.4L氧气的物质的量,故A错误;
B.56g铁的物质的量为1mol,1mol铁与足量氯气反应失去3mol电子,反应转移的电子数为3NA,故B错误;
C.4g氦气的物质的量为1mol,1mol氦气含有1mol原子,含有氦原子的个数为NA,故C正确;
D.没有告诉1mol?L-1 MgCl2溶液的体积,无法计算溶液中氯离子的物质的量及数目,故D错误;
故选C.
B.56g铁的物质的量为1mol,1mol铁与足量氯气反应失去3mol电子,反应转移的电子数为3NA,故B错误;
C.4g氦气的物质的量为1mol,1mol氦气含有1mol原子,含有氦原子的个数为NA,故C正确;
D.没有告诉1mol?L-1 MgCl2溶液的体积,无法计算溶液中氯离子的物质的量及数目,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项D为易错点,注意分析题中数据是否齐全.

练习册系列答案
相关题目
在“绿色化学”工艺中,理想状态是反应中原子全部转化为欲制的产物,即原子利用率为100%.下列反应最符合“绿色化学”要求的是( )
A、Cu+2H2SO4(浓)
| ||||
B、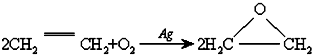 | ||||
| C、3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O | ||||
D、 |
对于反应Zn+H2SO4═ZnSO4+H2↑,下列措施不能增大氢气生成速率的是( )
| A、使用18.4mol?L-1的硫酸 |
| B、升高溶液的温度 |
| C、向溶液中加入少量铜粉 |
| D、把锌块(片)换成锌粉 |
有关物质的分类中,说法错误的是( )
| A、KNO3属于硝酸盐 |
| B、CaO属于氧化物 |
| C、NaHCO3属于酸 |
| D、Na2CO3属于钠盐 |


 小明为测定某牙膏中碳酸钙的质量分数,取该牙膏25克,加入200mL稀盐酸,恰好完全反应(其他成分不与盐酸反应),共收集到标准状况下3.36L二氧化碳气体,请通过计算说明:
小明为测定某牙膏中碳酸钙的质量分数,取该牙膏25克,加入200mL稀盐酸,恰好完全反应(其他成分不与盐酸反应),共收集到标准状况下3.36L二氧化碳气体,请通过计算说明: