题目内容
【题目】现有MgCl2和Al2(SO4)3的混合溶液,向其中逐滴加入NaOH溶液,得到沉淀的物质的量与加入NaOH的物质的量关系如图所示,则原溶液中Cl-与SO42-的物质的量之比为( )

A.4∶3B.1∶3C.1∶4D.2∶3
【答案】D
【解析】
首先写出发生镁离子和铝离子与氢氧根反应的离子方程式,然后发生反应氢氧化铝的溶解,由图可知,溶解Al(OH)3消耗氢氧化钠溶液的物质的量为0.1mol,根据离子方程式,可知沉淀Al3+消耗的氢氧化钠溶液的物质的量,沉淀Mg2+、Al3+总共消耗氢氧化钠溶液0.5mol,计算沉淀Mg2+消耗的氢氧化钠溶液的物质的量,据此确定溶液中SO42-与Cl-的物质的量之比。
首先发生反应Mg2++2OH═Mg(OH)2↓、Al3++3OH═Al(OH)3↓,然后发生反应Al(OH)3+OH═AlO2+2H2O,由图可知,溶解Al(OH)3消耗氢氧化钠溶液的物质的量为0.1mol,根据离子方程式Al3++3OH═Al(OH)3↓可知,沉淀Al3+消耗的氢氧化钠溶液的物质的量为0.1mol×3=0.3mol,沉淀Mg2+、Al3+总共消耗氢氧化钠溶液0.4mol,则沉淀Mg2+消耗的氢氧化钠溶液的物质的量为0.4mol0.3mol=0.1mol,Mg2++2OH═Mg(OH)2↓、Al3++3OH═Al(OH)3↓,则n(Mg2+):n(Al3+)=![]() :
:![]() =1:2,根据MgCl2和Al2(SO4)3的化学式,故Cl与SO42的物质的量之比为:1×2:2×
=1:2,根据MgCl2和Al2(SO4)3的化学式,故Cl与SO42的物质的量之比为:1×2:2×![]() =2:3,
=2:3,
答案选D。

 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案【题目】碱式碳酸铋片[主要成分(BiO)2CO3]可用于治疗慢性胃炎及缓解胃酸过多引起的胃病。由菱铋矿(主要成分为nBi2O3·mCO2·H2O,含杂质SiO2、CuS等)制备(BiO)2CO3的一种工艺如图:
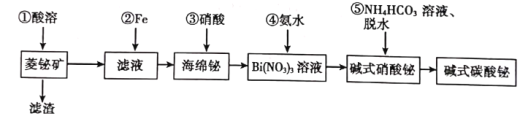
试回答下列问题:
(1)为提高①的“酸溶”速率,可以采取的措施是__________(任写一种)。
(2)①中酸溶解率与接触时间及溶液的pH之间的关系如图,据此分析,“酸溶”的最佳条件为__________;滤渣的主要成分是__________。
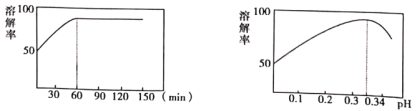
(3)“酸溶”后溶液必须保持强酸性,以防止铋元素流失,原理是__________。
(4)②中得到“海绵铋”的离子方程式为__________。
(5)④中反应的化学反应方程式为__________。
(6)25℃时,向浓度均为0.1mol·L-1的Fe2+、Cu2+、Bi3+的混合溶液中滴加Na2S溶液,当Fe2+恰好沉淀完全时,所得溶液c(Cu2+):c(Bi3+)=__________。(忽略Na2S溶液所带来的体积变化)。
资料:①有关溶度积数据见表:
难溶物质 | FeS | CuS | Bi2S3 |
Ksp(25℃) | 6.3×10-18 | 6.3×10-36 | 1.6×10-20 |
②溶液中的离子浓度小于等于10-5mol·L-1时,认为该离子沉淀完全。
【题目】某学生做同主族元素性质递变规律的实验时,自己设计了一套实验方案,并记录了有关实验现象.现在请你帮助该学生整理并完成实验报告.
(1)实验目的: ______
(2)实验用品:药品:氯水、溴水、溴化钠溶液、碘化钾溶液、四氯化碳.
仪器:① ______ ;② ______ ![]() 请填写两件主要的玻璃仪器
请填写两件主要的玻璃仪器![]()
(3)实验内容:
序号 | 实验方案 | 实验现象 |
① | 将少量氯水滴入盛有少量NaBr溶液的试管中,振荡;再滴入少量四氯化碳,振荡 | 加入氯水后,溶液由无色变为橙色,滴入四氯化碳后,水层颜色变浅,四氯化碳层 |
② | 将少量溴水滴入盛有少量KI溶液的试管中,振荡;再滴入少量四氯化碳,振荡 | 加入溴水后,溶液由无色变为黄色,滴入四氯化碳后,水层颜色变浅,四氯化碳层 |
(4)实验结论: ______ .
(5)问题和讨论:请用结构理论简单说明得出上述结论的原因. ______ .