题目内容
20.下列有关物质用途的说法不正确的是( )| A. | Na2O2用作呼吸面具的供氧剂 | B. | Al(OH)3用作制胃酸的中和剂 | ||
| C. | FeCl3用作铜制线路板的蚀刻剂 | D. | 浓硫酸用作NH3的干燥剂 |
分析 A.过氧化钠与水、二氧化碳反应生成氧气,氧化钠与水、二氧化碳反应不生成氧气;
B.氢氧化铝难溶于水,和胃酸发生反应可以治疗胃酸过多;
C.三价铁离子的氧化性大于铜离子,氯化铁可以溶解线路板上的金属铜;
D.氨水呈碱性,与浓硫酸发生反应;
解答 A.过氧化钠与水、二氧化碳反应生成氧气,所以过氧化钠用作供氧剂,故A正确;
B.氢氧化铝腐蚀性小能和胃酸反应,可以治疗胃酸过多,故B正确;
C.三价铁离子的氧化性大于铜离子,所以可用FeCl3溶液腐蚀线路板上的Cu,2FeCl3+Cu=2FeCl2+CuCl2,故C正确;
D.氨水呈碱性,与浓硫酸发生反应,所以不能用浓硫酸干燥氨气,故D错误;
故选D.
点评 本题考查了化学在生活中的应用,明确反应的实质和产物是解题关键,题目较简单.

练习册系列答案
相关题目
6.下列气体中,有毒、能污染大气,可以用氢氧化钠溶液吸收的是( )
| A. | Cl2 | B. | CO2 | C. | CO | D. | NH4 |
11.常温时,下列溶液的pH大于8的是( )
| A. | pH=6的盐酸用水稀释100倍 | |
| B. | pH=10的氨水用水稀释100倍 | |
| C. | pH=10的氢氧化钠溶液稀释1000倍 | |
| D. | 0.1 mol•L-1的硫酸100 mL跟0.2 mol•L-1 NaOH溶液100 mL完全反应 |
8.太空探索器常用${\;}_{94}^{238}$Pu制成的核电池提供动力,该钚原子的中子数为( )
| A. | 332 | B. | 238 | C. | 144 | D. | 94 |
15.下列实验方法或操作正确的是( )
| A. |  萃取碘水中碘 萃取碘水中碘 | B. |  过滤 | C. |  制取乙酸乙酯 制取乙酸乙酯 | D. |  制取淡水 制取淡水 |
5.短周期主族元素X、Y、Z、W的原子序数依次增大,四种元素的原子K层电子数总和为7,L层电子数总和为22,M层电子数总和为12.下列说法正确的是( )
| A. | 最高正价由低到高的顺序为:X、Z、Y、W | |
| B. | 原子半径由小到大的顺序为:X、Y、Z、W | |
| C. | 最外层电子数由少到多的顺序为:X、Z、Y、W | |
| D. | 简单氢化物的稳定性由弱到强的顺序为:Y、Z、W |
12.下列实验中,所采取的分离方法与对应原理都正确的是( )
| 选项 | 实验目的 | 分离方法 | 原理 |
| A | 除去CO2中的HCl | 通入饱和Na2CO3溶液 | HCl和Na2CO3溶液反应生成CO2 |
| B | 除去乙醇中少量的乙酸 | 加入足量生石灰蒸馏 | 乙醇和乙酸钙的沸点相差较大 |
| C | 除去KNO3固体中NaCl | 冷却热饱和溶液重结晶 | NaCl在水中的溶解度很大 |
| D | 分离乙酸和乙醇 | 用分液漏斗分液 | 乙醇乙酯和乙醇的密度不同 |
| A. | A | B. | B | C. | C | D. | D |
9.如图所示装置可用于(需要时可以用酒精灯加热)( )
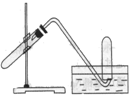

| A. | 加热NaHCO3制取和收集CO2 | |
| B. | 用铜和稀硝酸反应制取和收集NO | |
| C. | 用NH4Cl与浓NaOH溶液反应制取和收集NH3 | |
| D. | 用铜和浓硝酸反应制取和收集NO2 |
10.下列物质中,属于纯净物的是( )
| A. | 液氯 | B. | 铝热剂 | C. | 漂白粉 | D. | 水玻璃 |