��Ŀ����
| |||||||||||
�𰸣�
������
������
(1) |
��CO32��+CO2+H2O====2HCO3�� ��HCO3��+OH��====CO32��+H2O |
(2) |
����H2SO4��1�֣�SO3��1�֣� SO2��1�֣� ������������Cu+2H2SO4(Ũ) �� CuSO4+SO2��+2H2O��2�֣� ����HNO3��1�֣� NO2��1�֣�����NO��1�֣� ���� 3Cu+8HNO3(ϡ) ==== 3Cu(NO3)2+2NO��+4H2O��2�֣� ���� ��bΪHNO3 aΪNO cΪNO2 ���� Cu+4HNO3(Ũ) ====Cu(NO3)2+2NO2��+2H2O |

��ϰ��ϵ�д�
 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�
�����Ŀ
 ��֪b�����Ǻ�°����������ġ������ǡ��Ʋ�����ʽ����ʡ�д����Ӧ�����ӷ���ʽ��
��֪b�����Ǻ�°����������ġ������ǡ��Ʋ�����ʽ����ʡ�д����Ӧ�����ӷ���ʽ��

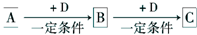
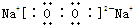
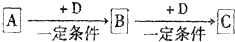 ��֪A��B��C����ѧ��ѧ�ij������ʣ�������һ������������ͼ��ʾת����ϵ��
��֪A��B��C����ѧ��ѧ�ij������ʣ�������һ������������ͼ��ʾת����ϵ��