题目内容
13.己烯雌酚是一种激素类药物,其结构简式如图所示,下列有关叙述中错误的是( )
| A. | 己烯雌酚的分子式为C18H20O2 | |
| B. | 己烯雌酚分子中所有碳原子一定不在同一平面内 | |
| C. | 己烯雌酚分子可与溴水发生加成反应 | |
| D. | 1 mol己烯雌酚分子与氢气在一定条件下完全反应时,最多可消耗7 mol H2 |
分析 由结构可知分子式,分子中含酚-OH、碳碳双键,结合酚、烯烃的性质来解答.
解答 解:A.己烯雌酚的分子式为C18H20O2,故A正确;
B.苯环、碳碳双键为平面结构,且直接相连,乙基与双键相连,则所有碳原子可能在同一平面内,故B错误;
C.含碳碳双键,可与溴水发生加成反应,故C正确;
D.苯环、双键均与氢气发生加成反应,则1 mol己烯雌酚分子与氢气在一定条件下完全反应时,最多可消耗7 mol H2,故D正确;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意常见有机物的性质,选项B为易错点,题目难度不大.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
16.以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
(1)卡片中记录合理的是③④⑥(填序号)
(2)该电池总反应的离子方程式是Zn+2H+=Zn2++H2↑
(3)若将稀硫酸换成硫酸铜溶液,电极质量增加的是铜极 (填“锌极”或“铜极”)
| ①Zn为正极,Cu为负极 ②H+向负极移动 ③Cu极有H2产生 ④电子流动方向Zn→Cu ⑤正极的电极反应式是Zn-2e-=Zn2+ ⑥若有1mol电子流过导线,则理论上产生0.5mol H2 |
(2)该电池总反应的离子方程式是Zn+2H+=Zn2++H2↑
(3)若将稀硫酸换成硫酸铜溶液,电极质量增加的是铜极 (填“锌极”或“铜极”)
1.某研究性学习小组进行电化学实验,研究装置如图所示.有关说法不正确的是( )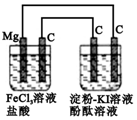

| A. | 电解池中阳极区溶液变红,阴极区溶液变蓝 | |
| B. | 原电池中碳极的电极反应式为:Fe3++e-═Fe2+ | |
| C. | 镁为负极,发生氧化反应 | |
| D. | 电解池中阴极的电极反应式为:2H++e-═H2↑ |
8.将106g Na2 CO3溶于1L水所得溶液与1mol Na2CO3溶于水稀释成1L的溶液相比,下列各量一定相等的是( )
| A. | 物质的量浓度 | B. | 溶液的密度 | C. | 溶质的质量 | D. | 溶质的质量分数 |
18.汽车的启动电源常用铅蓄电池,放电时的电池反应:PbO2+Pb+2H2SO4═2PbSO4+2H2O,下列说法正确的是( )
| A. | PbO2是电池的负极 | |
| B. | 正极反应式为:Pb+SO42--2e-═PbSO4 | |
| C. | H2SO4起传导电子的作用 | |
| D. | 电池放电时,溶液pH增大 |
5. 葡萄可用于酿酒.
葡萄可用于酿酒.
(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是产生红色沉淀.
(2)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备.实验室用下图所示装置制备乙酸乙酯:
①试管a中生成乙酸乙酯的化学方程式是CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O.
②实验开始时,试管b中的导管不伸入液面下的原因是防止溶液倒吸.
(3)有机物E由碳、氢、氧三种元素组成,可由葡萄糖发酵得到,也可从酸牛奶中提取,纯净的E为无色粘稠液体,易溶于水.为研究E的组成与结构,进行了如下实验:
④写出E与NaHCO3溶液反应的化学方程式HOOC-CH(OH)-CH3+NaHCO3=NaOOC-CH(OH)-CH3+H2O+CO2↑.
 葡萄可用于酿酒.
葡萄可用于酿酒.(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是产生红色沉淀.
(2)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备.实验室用下图所示装置制备乙酸乙酯:
①试管a中生成乙酸乙酯的化学方程式是CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O.
②实验开始时,试管b中的导管不伸入液面下的原因是防止溶液倒吸.
(3)有机物E由碳、氢、氧三种元素组成,可由葡萄糖发酵得到,也可从酸牛奶中提取,纯净的E为无色粘稠液体,易溶于水.为研究E的组成与结构,进行了如下实验:
| ①称取E4.5g,升温使其汽化,测其密度是相同条件下H2的45倍. | ①有机物E的相对分子量为:90 |
| ②将此9.0gE在足量纯O2充分燃烧,并使其产物依次通过碱石灰、无水硫酸铜粉末、足量石灰水,发现碱石灰增重14.2g,硫酸铜粉末没有变蓝,石灰水中有10.0g白色沉淀生成;向增重的碱石灰中加入足量盐酸后,产生4.48L无色无味气体(标准状况). | ②9.0g有机物E完全燃烧时,经计算:生成CO2共为0.3 mol |
| ③经红外光谱测定,证实其中含有羟基,羧基,甲基 |
16.下列说法不正确的是( )
| A. | 化学反应必然伴随发生能量变化 | |
| B. | 石灰石烧制石灰是吸热反应 | |
| C. | 反应的活化能越大,该化学反应前后的能量变化就越大 | |
| D. | 将AgNO3溶液滴加到KC1溶液中,反应的活化能几乎为零 |
17.在下列反应中属于氧化还原反应且水做还原剂的是( )
| A. | Cl2+H2O=HCl+HClO | B. | 2H2O+2F2=4HF+O2 | ||
| C. | ICl+H2O=HCl+HIO | D. | 2Na+2H2O=2NaOH+H2↑ |