题目内容
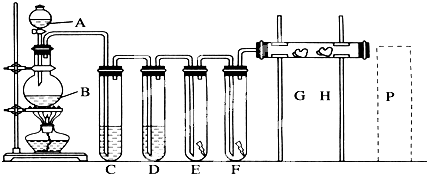
实验室用下述装置制取氯气,并用氯气进行下列实验. 回答下列问题:
(1)A、B两仪器的名称:A ,B .B中发生反应的化学方程式为 .
(2)洗气装置C是为了除去Cl2中的HCl气体,应放入的试剂是 ,D中浓H2SO4的作用是 .
(3)E中为红色干布条,F中为红色湿布条,可看到有色布条褪色的是 _.(填E或F)
(4)G是浸有淀粉KI溶液的棉花球,G处现象是棉花球表面变成 .H是浸有NaBr溶液的棉花球,H处反应的化学方程式是 .
(5)P处为尾气吸收装置,写出实验室吸取Cl2的化学方程式: .
(1)A、B两仪器的名称:A
(2)洗气装置C是为了除去Cl2中的HCl气体,应放入的试剂是
(3)E中为红色干布条,F中为红色湿布条,可看到有色布条褪色的是
(4)G是浸有淀粉KI溶液的棉花球,G处现象是棉花球表面变成
(5)P处为尾气吸收装置,写出实验室吸取Cl2的化学方程式:

考点:氯气的实验室制法
专题:
分析:(1)分析装置图中仪器作用和图形写出名称;
(2)浓盐酸易挥发,从发生装置中制取的氯气含有杂质氯化氢、水蒸气,氯气在饱和食盐水中溶解度不大,氯化氢极易溶于水,可用饱和食盐水吸收氯化氢;浓硫酸具有吸水性;
(3)氯气不具有漂白性,氯气与水反应生成的次氯酸具有漂白性;
(4)氯气具有强的氧化性,能够氧化碘离子和溴离子,单质碘遇到淀粉变蓝;
(5)氯气有毒,能够与氢氧化钠反应生成氯化钠、次氯酸钠和水,可以用氢氧化钠溶液吸收氯气.
(2)浓盐酸易挥发,从发生装置中制取的氯气含有杂质氯化氢、水蒸气,氯气在饱和食盐水中溶解度不大,氯化氢极易溶于水,可用饱和食盐水吸收氯化氢;浓硫酸具有吸水性;
(3)氯气不具有漂白性,氯气与水反应生成的次氯酸具有漂白性;
(4)氯气具有强的氧化性,能够氧化碘离子和溴离子,单质碘遇到淀粉变蓝;
(5)氯气有毒,能够与氢氧化钠反应生成氯化钠、次氯酸钠和水,可以用氢氧化钠溶液吸收氯气.
解答:
解:(1)装置图中仪器作用和图形可知是利用分液漏斗向烧瓶中加入浓盐酸加热反应生成氯气的发生装置;
故答案为:分液漏斗;圆底烧瓶;
(2)从发生装置出来的氯气中含有杂质HCl和水蒸气,通过盛有饱和食盐水的洗气瓶除去HCl,通过盛有浓硫酸的洗气瓶除去氯气中的水蒸气;
故答案为:饱和食盐水;吸收氯气中的水蒸气;
(3)氯气不具有漂白性,氯气与水反应生成的次氯酸具有漂白性,所以氯气能使湿润的有色布条褪色,不能使干燥的有色布条褪色,所以E中无变化,F中红色布条褪色;
故答案为:F;
(4)氯气和碘化钾溶液中的碘离子反应生成碘单质.碘遇到淀粉变蓝;Cl2也能将Br-氧化为Br2,离子方程式为:2NaBr+Cl2=2NaCl+Br2;
故答案为:蓝色;2NaBr+Cl2=2NaCl+Br2;
(5)氯气有毒,能够与氢氧化钠反应生成氯化钠、次氯酸钠和水,化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O;
故答案为:Cl2+2NaOH=NaCl+NaClO+H2O.
故答案为:分液漏斗;圆底烧瓶;
(2)从发生装置出来的氯气中含有杂质HCl和水蒸气,通过盛有饱和食盐水的洗气瓶除去HCl,通过盛有浓硫酸的洗气瓶除去氯气中的水蒸气;
故答案为:饱和食盐水;吸收氯气中的水蒸气;
(3)氯气不具有漂白性,氯气与水反应生成的次氯酸具有漂白性,所以氯气能使湿润的有色布条褪色,不能使干燥的有色布条褪色,所以E中无变化,F中红色布条褪色;
故答案为:F;
(4)氯气和碘化钾溶液中的碘离子反应生成碘单质.碘遇到淀粉变蓝;Cl2也能将Br-氧化为Br2,离子方程式为:2NaBr+Cl2=2NaCl+Br2;
故答案为:蓝色;2NaBr+Cl2=2NaCl+Br2;
(5)氯气有毒,能够与氢氧化钠反应生成氯化钠、次氯酸钠和水,化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O;
故答案为:Cl2+2NaOH=NaCl+NaClO+H2O.
点评:本题考查了实验室制备氯气的发生装置、除杂、性质检验、尾气处理的分析判断,明确氯气制备原理和氯气的性质是解题关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验能达到预期目的是( )
| A、检验溶液中是否含有CO32-:滴加稀盐酸,将产生的气体通入澄清石灰水 |
| B、检验溶液中是否含有SO42-:先滴加氯化钡溶液,再滴加稀盐酸 |
| C、检验溶液中是否含有Fe2+:先滴加氯水,再滴加KSCN溶液 |
| D、检验溶液中是否含有NH4+:先滴加浓NaOH溶液并加热,再用湿润的红色石蕊试纸 |
下列水溶液中,能大量共存的一组离子是( )
| A、Na+、H+、NO3-、SO32- |
| B、K+、H+、SO42-、CH3COO- |
| C、Mg2+、NH4+、SO42-、Cl- |
| D、K+、Fe3+、Cl-、SCN- |
 如图的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液.挤压胶管的胶头,下列与实验事实不相符的是( )
如图的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液.挤压胶管的胶头,下列与实验事实不相符的是( )| A、NH3(H2O含石蕊) 蓝色喷泉 |
| B、HCl (H2O含石蕊) 红色喷泉 |
| C、C12(饱和食盐水) 无色喷泉 |
| D、CO2(NaOH溶液) 无色喷泉 |
下列说法正确的是( )
| A、利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
| B、水电站把机械能转化成电能,而核电站把化学能转化成电能 |
| C、在医院中,为酸中毒病人输液应采用0.9%氯化铵溶液 |
| D、棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2O |
下列物质既能导电又是电解质的是( )
| A、无水乙醇 | B、液氯 |
| C、硫酸铜溶液 | D、熔融的KCl |
关于下列装置的说法正确的是( )
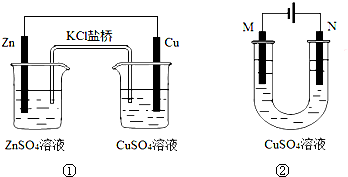

| A、装置①中盐桥内的K+移向CuSO4溶液 |
| B、装置①将电能转变为化学能 |
| C、若装置②用于铁棒镀铜,则N极为铁棒 |
| D、若装置②用于电解精炼铜,溶液中的Cu2+浓度保持不变 |