题目内容
6.某有机物的分子结构如下: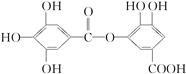 ,关于它的性质叙述中不正确的是( )
,关于它的性质叙述中不正确的是( )| A. | 酸性条件下可发生水解反应,且产物只有一种 | |
| B. | 1mol该有机物最多可跟8molNaOH反应 | |
| C. | 1mol该有机物最多可跟2molBr2反应 | |
| D. | 该有机物可跟NaHCO3溶液反应 |
分析 由结构可知,分子中含酚-OH、-COOH、-COOC-,结合酚、羧酸、酯的性质来解答.
解答 解:A.含-COOC-可发生水解反应,水解产物只有一种,水解产物中苯环上含3个酚-OH,且与中间-OH相对的C上有-COOH,故A正确;
B.5个酚-OH、1个-COOH、-COOC-及水解生成酚酚-OH均与NaOH反应,则1mol该有机物最多可跟8molNaOH反应,故B正确;
C.酚-OH的邻对位与溴水发生取代反应,则1mol该有机物最多可跟4molBr2反应,故C错误;
D.含-COOH,可跟NaHCO3溶液反应,故D正确;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意酚、羧酸、酯的性质,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.实验室常利用甲醛法测定某(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH${\;}_{4}^{+}$+6HCHO=4H++(CH2)6N4+6H2O,然后用NaOH标准溶液滴定反应生成的酸.某兴趣小组用甲醛法进行了如下实验:
步骤1.用电子天平准确称取样品1.5000g.
步骤2.将样品溶解并冷却后,完全转移到250mL容量瓶中,定容,充分摇匀.
步骤3.移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛,摇匀、静置5min,加入2滴酚酞试液,用NaOH标准溶液滴定到终点.重复步骤③操作2次.
(1)根据步骤3填空:
①下列操作可导致结果偏高的是BC.
A.读取滴定终点时NaOH溶液的体积时俯视刻度线
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
D.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
②滴定时边滴边摇动锥形瓶,眼睛应观察.
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化
③滴定达到终点时,溶液由无色色变为粉红(或浅红)色,且半分钟内不褪色.
④配制样品溶液及滴定实验中所需的玻璃仪器除烧杯、250mL容量瓶、锥形瓶、量筒、滴定管外,还有玻璃棒、胶头滴管.(填仪器名称)
(2)滴定结果如下表所示:
若NaOH标准溶液的浓度为0.1000mol•L-1,则该样品中氮的质量分数为18.76%.(保留两位小数)
步骤1.用电子天平准确称取样品1.5000g.
步骤2.将样品溶解并冷却后,完全转移到250mL容量瓶中,定容,充分摇匀.
步骤3.移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛,摇匀、静置5min,加入2滴酚酞试液,用NaOH标准溶液滴定到终点.重复步骤③操作2次.
(1)根据步骤3填空:
①下列操作可导致结果偏高的是BC.
A.读取滴定终点时NaOH溶液的体积时俯视刻度线
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
D.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
②滴定时边滴边摇动锥形瓶,眼睛应观察.
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化
③滴定达到终点时,溶液由无色色变为粉红(或浅红)色,且半分钟内不褪色.
④配制样品溶液及滴定实验中所需的玻璃仪器除烧杯、250mL容量瓶、锥形瓶、量筒、滴定管外,还有玻璃棒、胶头滴管.(填仪器名称)
(2)滴定结果如下表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.04 |
| 2 | 25.00 | 1.00 | 21.00 |
| 3 | 25.00 | 1.20 | 21.21 |
11.下列说法正确的是( )
| A. | 按系统命名法,有机物 可命名为2,6-二甲基-5-乙基辛烷 可命名为2,6-二甲基-5-乙基辛烷 | |
| B. | 若某高聚物对应的单体只有一种,则此高聚物与单体有相同的最简式 | |
| C. | 等质量的甲烷、乙烯、1,3-丁二烯分别充分燃烧,所耗用氧气的量依次减少 | |
| D. | 用甘氨酸(H2N-CH2-COOH)和丙氨酸( )缩合最多可形成3种二肽 )缩合最多可形成3种二肽 |
18.已知短周期元素的离子aA3+、bB+、cC2-、dD-都具有相同的电子层结构,下列关系正确的是( )
| A. | 质子数:c>b | B. | 离子的还原性:C2-<D- | ||
| C. | 氢化物的稳定性:H2C>HD | D. | 离子半径:B+>A3+ |
15.下列说法中错误的是( )
| A. | 若XY4分子中X原子处于正四面体的中心,则XY4分子为非极性分子 | |
| B. | C2H5OH与C2H5Br相比,前者的相对分子质量远小于后者,而沸点却远高于后者,其原因是前者的分子间存在氢键 | |
| C. | CO2与SiO2晶体熔化时,所克服的微粒间相互作用不同 | |
| D. | 短周期元素离子aXn-和bYm-具有相同的电子层结构,若a>b,则n>m |
 如图转化关系图(反应条件均略去)中A、C、E、G均为单质,其中A、C、G为金属;E为气体;B为无色液体;A、G在冷的浓硫酸溶液中均发生钝化;F、I溶液的焰色均为黄色.
如图转化关系图(反应条件均略去)中A、C、E、G均为单质,其中A、C、G为金属;E为气体;B为无色液体;A、G在冷的浓硫酸溶液中均发生钝化;F、I溶液的焰色均为黄色.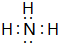 ,结构式为
,结构式为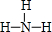 ,写出D的气态氢化物在催化剂存在下跟氧气反应的化学方程式4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
,写出D的气态氢化物在催化剂存在下跟氧气反应的化学方程式4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O. .
. 如图是一个用铂丝作电极,电解Na2SO4溶液的装置,电解液中加有酚酞.闭合开关,电解一段时间后发现:a、b试管中产生气体的体积比为2:1.
如图是一个用铂丝作电极,电解Na2SO4溶液的装置,电解液中加有酚酞.闭合开关,电解一段时间后发现:a、b试管中产生气体的体积比为2:1.