题目内容
为了除去粗食盐中Ca2+、Mg2+、SO42-离子及泥砂等不溶性杂质,将粗食盐溶于水后,经下列步骤将粗盐制成精盐.①加入稍过量的BaCl2溶液;②加入稍过量的NaOH溶液;③加入稍过量的Na2CO3溶液;④过滤;⑤滴入稀盐酸至无气泡产生;⑥蒸发、结晶.回答下列有关问题.
(1)过滤时,用到的主要玻璃仪器有 ;
(2)操作①后,检验溶液中SO42-是否除尽的方法是 ;
(3)操作③的目的是 ,操作⑤目的是 ;
(4)操作①②能否颠倒 ,①③能否颠倒 ;(填“能”与“否”)操作④除掉的杂质为 .
(1)过滤时,用到的主要玻璃仪器有
(2)操作①后,检验溶液中SO42-是否除尽的方法是
(3)操作③的目的是
(4)操作①②能否颠倒
考点:粗盐提纯
专题:实验题
分析:(1)过滤时,用到的主要玻璃仪器有漏斗、玻璃棒、烧杯;
(2)检验SO42-是否沉淀完全可以采用反滴法,故可以采用取上层清液少许于试管中,滴加BaCl2溶液,如无沉淀生成,则表明SO42-已沉淀完全;如有沉淀生成,则表明SO42-未沉淀完全;
(3)加入稍过量的Na2CO3溶液,可以除去Ca2+、Ba2+;滴入稀盐酸至无气泡产生,除去过量的NaOH、Na2CO3,
(4)Mg2+用过量的NaOH溶液除去,SO42-加入稍过量的BaCl2溶液除去,操作①②可以颠倒;①③不能颠倒,由于过量的Na2CO3溶液可以除掉Ca2+和过量的Ba2+,若颠倒,过量的Ba2+仍然需要除杂试剂皿;操作④除掉的杂质是BaSO4、CaCO3、Mg(OH)2.
(2)检验SO42-是否沉淀完全可以采用反滴法,故可以采用取上层清液少许于试管中,滴加BaCl2溶液,如无沉淀生成,则表明SO42-已沉淀完全;如有沉淀生成,则表明SO42-未沉淀完全;
(3)加入稍过量的Na2CO3溶液,可以除去Ca2+、Ba2+;滴入稀盐酸至无气泡产生,除去过量的NaOH、Na2CO3,
(4)Mg2+用过量的NaOH溶液除去,SO42-加入稍过量的BaCl2溶液除去,操作①②可以颠倒;①③不能颠倒,由于过量的Na2CO3溶液可以除掉Ca2+和过量的Ba2+,若颠倒,过量的Ba2+仍然需要除杂试剂皿;操作④除掉的杂质是BaSO4、CaCO3、Mg(OH)2.
解答:
解:(1)过滤时,用到的主要玻璃仪器有漏斗、玻璃棒、烧杯,
故答案为:漏斗、玻璃棒、烧杯;
(2)检验SO42-是否沉淀完全可以采用反滴法,故可以采用取上层清液少许于试管中,滴加BaCl2溶液,如无沉淀生成,则表明SO42-已沉淀完全;如有沉淀生成,则表明SO42-未沉淀完全.
故答案为:取上层清液少许于试管中,滴加BaCl2溶液,如无沉淀生成,则表明SO42-已沉淀完全;如有沉淀生成,则表明SO42-未沉淀完全;
(3)加入稍过量的Na2CO3溶液,可以除去Ca2+、Ba2+;滴入稀盐酸至无气泡产生,除去过量的NaOH、Na2CO3,
故答案为:除去Ca2+、Ba2+;除去过量的NaOH、Na2CO3;
(4)Mg2+用过量的NaOH溶液除去,SO42-加入稍过量的BaCl2溶液除去,操作①②可以颠倒;①③不能颠倒,由于过量的Na2CO3溶液可以除掉Ca2+和过量的Ba2+,若颠倒,过量的Ba2+仍然需要除杂试剂皿;操作④除掉的杂质是BaSO4、CaCO3、Mg(OH)2,
故答案为:能;不能;BaSO4、CaCO3、Mg(OH)2.
故答案为:漏斗、玻璃棒、烧杯;
(2)检验SO42-是否沉淀完全可以采用反滴法,故可以采用取上层清液少许于试管中,滴加BaCl2溶液,如无沉淀生成,则表明SO42-已沉淀完全;如有沉淀生成,则表明SO42-未沉淀完全.
故答案为:取上层清液少许于试管中,滴加BaCl2溶液,如无沉淀生成,则表明SO42-已沉淀完全;如有沉淀生成,则表明SO42-未沉淀完全;
(3)加入稍过量的Na2CO3溶液,可以除去Ca2+、Ba2+;滴入稀盐酸至无气泡产生,除去过量的NaOH、Na2CO3,
故答案为:除去Ca2+、Ba2+;除去过量的NaOH、Na2CO3;
(4)Mg2+用过量的NaOH溶液除去,SO42-加入稍过量的BaCl2溶液除去,操作①②可以颠倒;①③不能颠倒,由于过量的Na2CO3溶液可以除掉Ca2+和过量的Ba2+,若颠倒,过量的Ba2+仍然需要除杂试剂皿;操作④除掉的杂质是BaSO4、CaCO3、Mg(OH)2,
故答案为:能;不能;BaSO4、CaCO3、Mg(OH)2.
点评:本题考查在粗盐提纯的过程中所选用除杂和净化的方法,难度不大,除去杂质不要引入新的杂质,对于实验过程中过量的试剂都要除去.

练习册系列答案
相关题目
下列关于醛的说法中正确的是( )
| A、甲醛是甲基跟醛基相连而构成的醛 |
| B、醛的官能团是-COH |
| C、饱和一元脂肪醛的分子式符合CnH2nO |
| D、甲醛、乙醛、丙醛均无同分异构体 |
某链状有机物分子中含有n个-CH2-,m个 ,a个-CH3,其余为-OH,则羟基的个数为( )
,a个-CH3,其余为-OH,则羟基的个数为( )
 ,a个-CH3,其余为-OH,则羟基的个数为( )
,a个-CH3,其余为-OH,则羟基的个数为( )| A、2n+3m-a |
| B、m+2-a |
| C、n+m+a |
| D、m+2n+2-a |
 某有机物的结构为如图所示,这种有机物可能具有的性质是( )
某有机物的结构为如图所示,这种有机物可能具有的性质是( )①可以燃烧;②能使酸性KMnO4溶液褪色;③能跟NaOH溶液反应; ④能发生酯化反应;
⑤能发生加成反应.
| A、②③④⑤ | B、①②③④⑤ |
| C、①②③⑤ | D、①②④⑤ |
某有机物的结构简式如下,则下列说法正确的是( )


| A、1mol该有机物与足量的NaOH溶液混合共热,充分反应最多可消耗6mol NaOH |
| B、向该有机物溶液中加入FeCl3溶液,振荡后有紫色沉淀产生 |
| C、该有机物能发生消去反应 |
| D、该有机物在稀硫酸中加热水解,有机产物只有一种 |

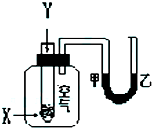 某学生用如图所示装置进行化学反应X+2Y═2Z能量变化情况的研究.当往试管中滴加试剂Y时,看到U型管中液面甲处降乙处升.关于该反应的下列叙述:
某学生用如图所示装置进行化学反应X+2Y═2Z能量变化情况的研究.当往试管中滴加试剂Y时,看到U型管中液面甲处降乙处升.关于该反应的下列叙述: